KEYTRUDA®(ペムブロリズマブ)、 高リスク早期トリプルネガティブ乳がんに対する術前補助化学療法との併用療法と それに続く術後のKEYTRUDA®単独補助療法としてFDAの承認を取得 高リスク早期トリプルネガティブ乳がん(TNBC)に対する初のがん免疫療法レジメン 米国におけるKEYTRUDA®の承認件数は30件に
2021/08/04 00:00 JST
報道関係各位
MSD株式会社
この参考資料は、FDA Approves KEYTRUDA® (pembrolizumab) for Treatment of Patients With High-Risk Early-Stage Triple-Negative Breast Cancer in Combination With Chemotherapy as Neoadjuvant Treatment, Then Continued as Single Agent as Adjuvant Treatment After Surgery の日本語訳であり、内容や解釈については英語が優先されます。適応症と安全性情報も米国のものであり、日本国内の情報ではありません。
KEYTRUDA®は、日本ではキイトルーダ®として、悪性黒色腫、切除不能な進行・再発の非小細胞肺癌、再発又は難治性の古典的ホジキンリンパ腫、がん化学療法後に増悪した根治切除不能な尿路上皮癌、がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性(MSI-High)を有する固形癌(標準的な治療が困難な場合に限る)注)、根治切除不能又は転移性の腎細胞癌、再発又は遠隔転移を有する頭頸部癌、がん化学療法後に増悪したPD-L1陽性の根治切除不能な進行・再発の食道扁平上皮癌に対する効能又は効果で承認を取得しております。 注)条件付き早期承認対象
参考資料
KEYTRUDA®(ペムブロリズマブ)、
高リスク早期トリプルネガティブ乳がんに対する術前補助化学療法との併用療法と
それに続く術後のKEYTRUDA®単独補助療法としてFDAの承認を取得
高リスク早期トリプルネガティブ乳がん(TNBC)に対する初のがん免疫療法レジメン
米国におけるKEYTRUDA®の承認件数は30件に
2021年7月27日 ニュージャージー州ケニルワース―Merck & Co., Inc., Kenilworth, N.J., U.S.A.(米国とカナダ以外ではMSD)は本日、抗PD-1抗体KEYTRUDA®が、第3相KEYNOTE-522試験に基づき、高リスク早期トリプルネガティブ乳がん(TNBC)に対する化学療法とKEYTRUDA®の併用療法による術前補助療法と、KEYTRUDA®の単独療法による術後補助療法として米国食品医薬品局(FDA)の承認を取得したことを発表しました。TNBCは再発率が高く、進行の速い乳がんです。KEYNOTE-522試験では、治療歴のないステージIIまたはステージIIIのTNBC患者に対する術前のKEYTRUDA®と化学療法(カルボプラチンおよびパクリタキセル、その後ドキソルビシンまたはエピルビシン+シクロホスファミド)の併用療法とそれに続く術後のKEYTRUDA®単独療法において、同様の術前補助化学療法のみの場合と比較して無イベント生存期間(EFS)が有意に改善し、根治手術ができない疾患進行、局所再発・遠隔転移、新たながんの発生、原因を問わない死亡のリスクが37%低減しました(HR=0.63 [95% CI, 0.48-0.82]; p=0.00031)。今回の承認により、米国におけるKEYTRUDA®の承認件数は30件となりました。
米国テキサス州ダラスにあるBaylor University Medical Center, Texas Oncology, U.S. Oncologyの乳がん研究部門責任者のJoyce O’Shaughnessy博士は、「TNBCは早期に診断されても30〜40%の患者さんが標準治療である術前補助療法と手術の後に再発します。このため、新たな治療の選択肢に対する高いアンメットニーズが存在します。本日の承認取得は非常に喜ばしいニュースであり、高リスク早期TNBCに対するレジメンにがん免疫療法が新たに加わったことで、治療のパラダイムが変わる可能性があります」と述べています。
重篤な、または死亡にいたる可能性のある免疫関連有害事象が様々な臓器や組織に発生する可能性があり、複数の臓器に同時に発生する場合もあります。KEYTRUDA®による治療中または治療後のあらゆる時点で、肺臓炎、大腸炎、肝炎、内分泌疾患、腎炎、皮膚反応、実質臓器移植の拒絶反応、同種造血幹細胞移植の合併症など、免疫関連の有害事象が発生する可能性があります。ここに列記する重大な免疫関連有害事象は、発生しうる重篤で命にかかわる免疫関連有害事象をすべて網羅しているわけではありません。KEYTRUDA®の安全な使用のためには、免疫関連有害事象の早期発見と管理が重要です。有害事象の重症度に応じてKEYTRUDA®の投与を休薬または中止し、適宜コルチコステロイドを投与します。KEYTRUDA®は重篤な、または命にかかわるinfusion reaction(点適時の過敏症反応)を引き起こす場合があります。
当社研究開発本部臨床研究担当バイスプレジデントであるVicki Goodman博士は、「トリプルネガティブ乳がんは、乳がんの中でも治療が困難であり、残念ながら特に米国では若い女性や黒人女性に多く見られます。この難治性のがんに直面する患者さんに新たな治療の選択肢を提供できることを誇りに思います。KEYTRUDA®を併用するこの術前・術後補助療法は、高リスク早期TNBCで初めて承認されたがん免疫療法のレジメンであり、乳がんコミュニティーにとって重要な節目となります」と述べています。
また、FDAが承認する検査で腫瘍にPD-L1発現(Combined Positive Score(CPS)≧10)の認められる切除不能の局所再発または転移性TNBCを適応症とするKEYTRUDA®と化学療法との併用療法に対する迅速承認について、FDAはKEYNOTE-522試験の確証データに基づき完全(通常)承認に移行しました。これは当初、第3相KEYNOTE-355試験の結果に基づき、2020年11月に承認されたものです。
当社は、婦人科がんおよび乳がんにおいてKEYTRUDA®をはじめとする様々な治験薬や承認薬を評価する広範な臨床開発プログラムを展開しており、これらのがんにおけるポートフォリオの拡充を迅速に進めています。
承認の元となったデータ
この承認は、新たに高リスク早期TNBCと診断された治療歴のない1,174名の患者(腫瘍径が1センチメートル[cm]超2cm以下でリンパ節転移を伴うもの、またはリンパ節転移の有無に関わらず腫瘍径が2cm超)を対象とする無作為化多施設共同二重盲検プラセボ対照KEYNOTE-522試験(ClinicalTrials.gov, NCT03036488 )のデータに基づくものです。被験者は腫瘍細胞におけるプログラム細胞死リガンド1(PD-L1)の発現に関わらず登録しました。治療の2年以内に活動性の自己免疫疾患の全身治療を受けた患者、免疫抑制を必要とする状態の患者は対象外でした。無作為化はリンパ節転移の有無(陽性・陰性)、腫瘍径(T1/T2、T3/T4)、カルボプラチンの投与間隔(3週間ごと、1週間ごと)で層別化されました。患者は次の治療群に2:1の割合で無作為に割り付けられ、薬剤はすべて静脈内投与されました
●第1群
- 術前にKEYTRUDA® 200 mg(治療レジメンの1〜4サイクル目の初日に3週間ごと)を、カルボプラチン(AUC(Area Under Curve) 5 mg/mL/minを治療レジメンの1〜4サイクル目の初日に3週間ごとまたはAUC 1.5 mg/mL/minを治療レジメンの1〜4サイクル目の初日、8日目、15日目に1週間ごと)およびパクリタキセル80 mg/m2(治療レジメンの1〜4サイクル目の初日、8日目、15日目に1週間ごと)とともに併用投与し、これを4サイクル実施
- さらに、術前にKEYTRUDA® 200 mg(治療レジメンの5〜8サイクル目の初日に3週間ごと)を、ドキソルビシン60mg/m2またはエピルビシン90mg/m2(治療レジメンの5〜8サイクル目の初日に3週間ごと)およびシクロホスファミド600mg/m2(治療レジメンの5〜8サイクル目の初日に3週間ごと)とともに併用投与し、これを4サイクル実施
- 術後にKEYTRUDA® 200 mgを3週間ごとに9サイクル投与
●第2群
- 術前にプラセボ(治療レジメンの1〜4サイクル目の初日に3週間ごと)を、カルボプラチン(AUC(Area Under Curve) 5 mg/mL/minを治療レジメンの1〜4サイクル目の初日に3週間ごとまたは AUC1.5 mg/mL/minを治療レジメンの1〜4サイクル目の初日、8日目、15日目に1週間ごと)およびパクリタキセル80 mg/m2(治療レジメンの1〜4サイクル目の初日、8日目、15日目に1週間ごと)とともに併用投与し、これを4サイクル実施
- さらに、術前にプラセボ(治療レジメンの5〜8サイクル目の初日に3週間ごと)を、ドキソルビシン60mg/m2またはエピルビシン90mg/m2(治療レジメンの5〜8サイクル目の初日に3週間ごと)およびシクロホスファミド600mg/m2(治療レジメンの5〜8サイクル目の初日に3週間ごと)とともに併用投与し、これを4サイクル実施
- 術後にプラセボを3週間ごとに9サイクル投与
主要評価項目は病理学的完全奏効(pCR)率とEFSでした。病理学的完全奏効率は、乳房およびリンパ節の浸潤がんが消失した状態(ypT0/Tis ypN0)とし、根治手術の際に治験実施医療機関の病理医が盲検下で評価しました。無イベント生存期間は無作為割り付け時から、根治手術ができない疾患進行、局所再発・遠隔転移、新たながんの発生、原因を問わない死亡のいずれかまでの時間としました。さらに全生存期間(OS)も評価項目としました。
試験集団特性の内訳は以下のとおりです。年齢の中央値49歳(範囲:22〜80歳)、65歳以上11%、女性99.9%、白人64%、アジア人20%、黒人4.5%、アメリカ先住民またはアラスカ先住民1.8%、ECOG PS 0の患者87%、ECOG PS 1の患者13%、閉経前患者56%、閉経後患者44%、原発腫瘍1(T1)7%、T2 68%、T3 19%、T4 7%、リンパ節転移0(N0)49%、N1 40%、N2 11%、N3 0.2%、総合ステージ(overall stage)II 75%、ステージIII 25%
認められた有効性:
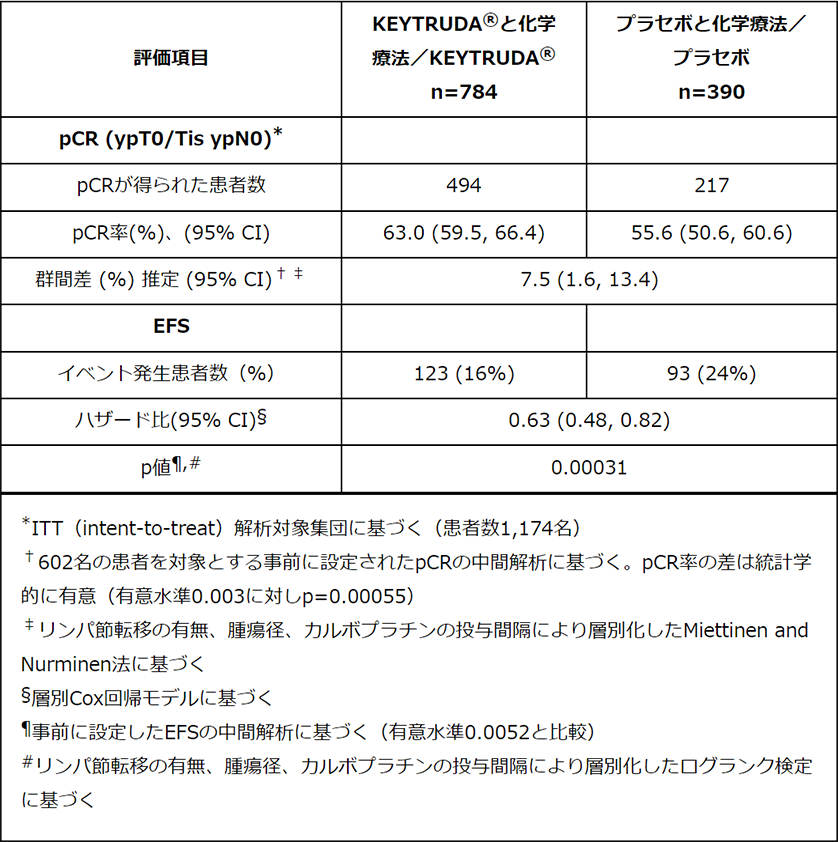
プロトコルで事前に設定されたOSの中間解析(4回目の中間解析)の時点で、OSは最終解析に必要なイベント数の45%で、データは未成熟でした。
この試験におけるKEYTRUDA®の投与期間の中央値は13.3カ月(範囲:1日〜21.9カ月)でした。死亡にいたった有害事象はKEYTRUDA®群の0.9%に発生し、急性副腎不全、自己免疫性脳炎、肝炎、肺炎、肺臓炎、肺塞栓症、多臓器機能不全症候群および心筋梗塞に伴う敗血症が1例ずつでした。重篤な有害事象はKEYTRUDA®群の44%に認められました。KEYTRUDA®群の2%以上の患者に認められた重篤な有害事象は、発熱性好中球減少症(15%)、発熱(3.7%)、貧血(2.6%)、好中球減少症(2.2%)でした。20%の患者が有害事象によりKEYTRUDA®の投与を中止しました。最も高頻度(1%以上)で認められ、KEYTRUDA®の投与の完全な中止にいたった有害事象は、アラニンアミノトランスフェラーゼ(ALT)の上昇(2.7%)、アスパラギン酸アミノトランスフェラーゼ(AST)の上昇(1.5%)、皮疹(1%)でした。57%の患者が有害事象によりKEYTRUDA®の投与を中断しました。最も高頻度(2%以上)で認められ、KEYTRUDA®の投与中断にいたった有害事象は、好中球減少症(26%)、血小板減少症(6%)、ALT上昇(6%)、AST上昇(3.7%)、貧血(3.5%)、皮疹(3.2%)、発熱性好中球減少症(2.8%)、白血球減少症(2.8%)、上気道感染(2.6%)、発熱(2.2%)、疲労(2.1%)でした。最も高頻度で認められた有害事象(全グレード、20%以上)は、疲労(70%)、悪心(67%)、脱毛(61%)、皮疹(52%)、便秘(42%)、下痢(41%)、末梢神経障害(41%)、口内炎(34%)、嘔吐(31%)、頭痛(30%)、関節痛(29%)、発熱(28%)、咳(26%)、腹痛(24%)、食欲減退(23%)、不眠症(21%)、筋肉痛(20%)でした。
トリプルネガティブ乳がん(TNBC)について
TNBCは診断から5年以内の再発率が高く、進行の速い乳がんです。乳がんにはエストロゲン受容体、プロゲステロン受容体のいずれかが陽性を示す、またはヒト上皮成長因子受容体2(HER2)が過剰発現しているタイプがありますが、TNBCではいずれも陰性となります。乳がん患者の約10〜15%がTNBCと診断されています。TNBCは40歳以下の女性、アフリカ系アメリカ人女性、BRCA1遺伝子変異を有する女性に多いとされています。
KEYTRUDA®について
KEYTRUDA®は、自己の免疫力を高め、がん細胞を見つけて攻撃するのを助ける抗PD-1抗体です。KEYTRUDA®はPD-1とそのリガンドであるPD-L1およびPD-L2との相互作用を阻害して、がん細胞を攻撃するT リンパ球を活性化するヒト化モノクローナル抗体です。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.は業界最大のがん免疫療法臨床研究プログラムを行っており、現在1,500を超えるKEYTRUDA®の臨床試験を実施し、幅広い種類のがんや治療セッティングを検討しています。KEYTRUDA®の臨床プログラムでは、さまざまながんにおけるKEYTRUDA®の役割や、KEYTRUDA®による治療効果が得られる可能性を予測する因子について模索しており、さまざまなバイオマーカーの模索も行っています。
KEYTRUDA®用法・用量・安全性情報・Access Program・患者支援プログラムについて
用法・用量・安全性情報・Access Program・患者支援プログラムなど一部情報は米国のもので、日本の情報ではありません。詳しくは当社英文リリースをご参照ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.のがん領域における取り組み
Merck & Co., Inc., Kenilworth, N.J., U.S.A.では、画期的な科学を革新的ながん治療薬に変換して世界中のがん患者さんを助けることに取り組んでいます。当社のオンコロジー事業にとって、がんと闘う人々を助けることは私たちの情熱であり、がん治療薬へアクセスしやすくすることは私たちの責任です。また、がん領域における取り組みの一環として、医薬品業界で一二を争う急成長を遂げている開発プログラムにより、30種類以上のがんに対するがん免疫療法の可能性を模索しています。また、引き続き戦略的買収を通じてポートフォリオを強化し、進行がんの治療を改善する可能性をもつ有望ながん治療薬候補の開発を最優先に進めています。当社のオンコロジー臨床試験について詳しくは、当社ウェブサイト をご覧ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.について
Merck & Co., Inc., Kenilworth, N.J., U.S.A.(米国とカナダ以外ではMSD)は130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。また、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続け、世界最高の研究開発型バイオ医薬品企業を目指しています。詳細については、当社ウェブサイトやTwitter、Facebook、Instagram、YouTube、LinkedInをご参照ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.の将来に関する記述
このニュースリリースには、米国の1995年私的証券訴訟改革法(the Private Securities Litigation Reform Act of 1995)の免責条項で定義された「将来に関する記述」が含まれています。これらの記述は、Merck & Co., Inc., Kenilworth, N.J., U.S.A.の経営陣の現時点での信条と期待に基づくもので、相当のリスクと不確実性が含まれています。新薬パイプラインに対する承認取得またはその製品化による収益を保証するものではありません。予測が正確性に欠けていた場合またはリスクもしくは不確実性が現実化した場合、実際の成果が、将来に関する記述で述べたものと異なる場合も生じます。
リスクと不確実性には、業界の一般的な状況および競争環境、金利および為替レートの変動などの一般的な経済要因、昨今の新型コロナウイルス感染症(COVID-19)の世界的大流行の影響、医薬品業界の規制やヘルスケア関連の米国法および国際法が及ぼす影響、ヘルスケア費用抑制の世界的な傾向、競合他社による技術的進歩や新製品開発および特許取得、承認申請などの新薬開発特有の問題、Merck & Co., Inc., Kenilworth, N.J., U.S.A.による将来の市況予測の正確性、製造上の問題または遅延、国際経済および政府の信用リスクなどの金融不安、画期的製品に対するMerck & Co., Inc., Kenilworth, N.J., U.S.A.の特許権やその他の保護の有効性への依存、特許訴訟や規制措置の対象となる可能性等がありますが、これらに限定されるものではありません。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.は、新たな情報、新たな出来事、その他いかなる状況が加わった場合でも、将来に関する記述の更新を行う義務は負いません。将来に関する記述の記載と大きく異なる成果を招くおそれがあるこの他の要因については、Merck & Co., Inc., Kenilworth, N.J., U.S.A.に関するForm 10-Kの2020年度年次報告書および米国証券取引委員会(SEC)のインターネットサイト(www.sec.gov)で入手できるSECに対するその他の書類で確認できます。
# # #
MSDについて
MSD(Merck & Co., Inc., Kenilworth, N.J., U.S.A.が米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。MSDはまた、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続けています。MSDは世界最高の研究開発型バイオ医薬品企業を目指しています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)やFacebook、Twitter、YouTubeをご参照ください。

