深在性真菌症治療剤「ノクサフィル®」の 効能又は効果の追加承認を取得
2021/09/27 00:00 JST
報道関係各位
MSD株式会社
MSD株式会社(本社:東京都千代田区、代表取締役社長:カイル・タトル、以下MSD)は、本日、深在性真菌症治療剤「ノクサフィル®錠100mg」および「ノクサフィル®点滴静注300mg」(一般名:ポサコナゾール)について、効能又は効果の真菌症の治療に「侵襲性アスペルギルス症」の追加承認を取得しましたのでお知らせいたします。ノクサフィル®は、アスペルギルス属やムーコル目にも抗真菌活性を示すアゾール系抗真菌剤で、真菌細胞の細胞膜を構成するエルゴステロールの生合成を阻害し、各種酵母様真菌および糸状菌に対して抗真菌作用を示します。
深在性真菌症は、臓器または全身性の重篤な感染症で、早期診断および早期治療が求められています。深在性真菌症の中で発現頻度が最も高いのは、アスペルギルス属による感染症であり、重篤例の割合も高いことが報告されています。現在利用可能な抗真菌薬で治療を行った場合でも、死亡率が高いなど、深在性真菌症は予後を左右する重症感染症です。診断が困難であり、発症すると予後が不良であるため、深在性真菌症のリスク因子である、同種造血幹細胞移植や好中球減少等がある患者では、抗真菌薬の予防投与が国内外のガイドラインで推奨されています。
ノクサフィル®は、既に「造血幹細胞移植患者又は好中球減少が予測される血液悪性腫瘍患者における深在性真菌症の予防」の効能又は効果の適応を取得していますが、今般、侵襲性アスペルギルス症に対する第一選択薬として国内外の診療ガイドラインで推奨されているボリコナゾールを対照薬に用いた国内第3相試験(深在性真菌症患者)および海外第3相試験(侵襲性アスペルギルス症患者)において、侵襲性アスペルギルス症患者に対する治療効果を示すことが確認されました。
ノクサフィル®は、既に承認されているムーコル症などの希少真菌症に対する治療選択肢としてだけでなく、侵襲性アスペルギルス症の治療においても新たな選択肢の一つとなることが期待されます。
MSDは、今後も感染症予防と治療に貢献し、日本における医療ニーズに応えてまいります。
以上
MSDについて
MSD(Merck & Co., Inc., Kenilworth, N.J., U.S.A.が米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。MSDはまた、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続けています。MSDは世界最高の研究開発型バイオ医薬品企業を目指しています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)や Facebook 、 Twitter 、 YouTubeをご参照ください。
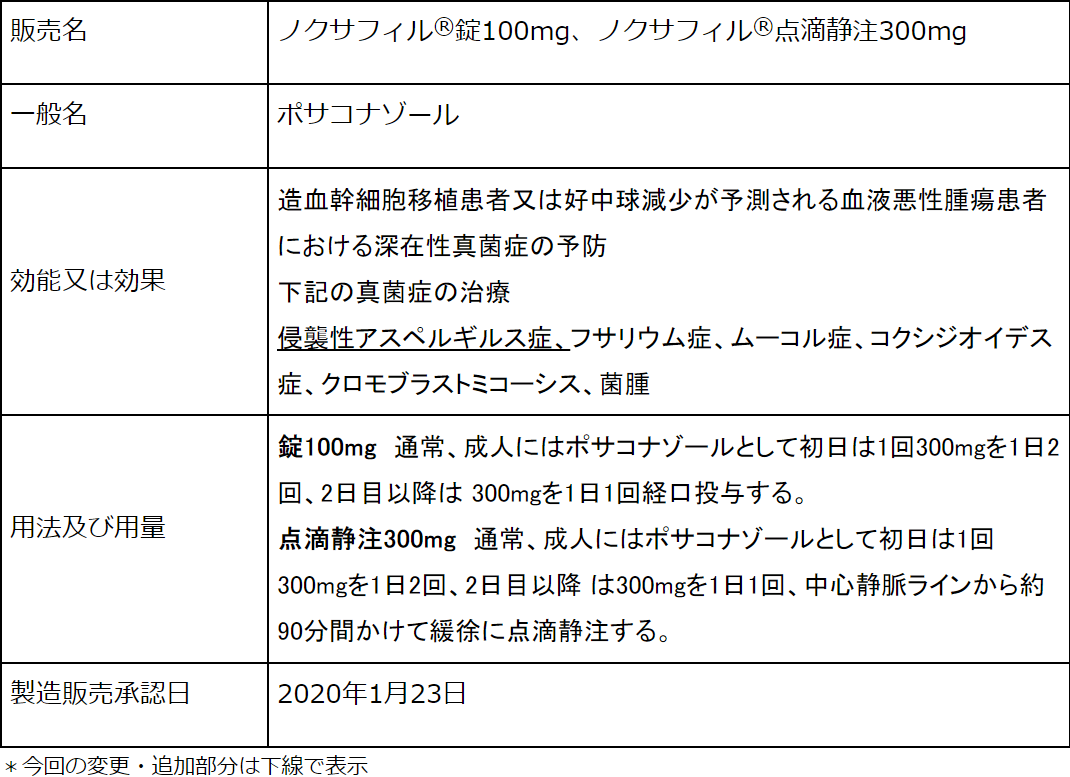
<参考資料>
製品概要