LYNPARZA®(オラパリブ)、アビラテロンとの併用療法が、 転移性去勢抵抗性前立腺がん(mCRPC)の一次治療において、バイオマーカーのステータスに かかわらず疾患進行または死亡のリスクをアビラテロンと比較して34%減少 PROpel試験は第3相試験として初めて、mCRPCの一次治療において PARP阻害剤との併用で画像診断に基づく無増悪生存期間の臨床的有用性を示す
2022/02/22 00:00 Asia/Tokyo
報道関係各位
MSD株式会社
この参考資料は、LYNPARZA® (olaparib) Plus Abiraterone Reduced Risk of Disease Progression or Death by 34% Versus Abiraterone in First-Line Metastatic Castration-Resistant Prostate Cancer, Regardless of Biomarker Status の日本語訳であり、内容や解釈については英語が優先されます。適応症と安全性情報も米国のものであり、日本国内の情報ではありません。
LYNPARZA®は、日本ではリムパーザ®として、白金系抗悪性腫瘍剤感受性の再発卵巣癌における維持療法、BRCA遺伝子変異陽性の卵巣癌における初回化学療法後の維持療法、相同組換え修復欠損を有する卵巣癌におけるベバシズマブ(遺伝子組換え)を含む初回化学療法後の維持療法、がん化学療法歴のあるBRCA遺伝子変異陽性かつHER2陰性の手術不能又は再発乳癌、BRCA遺伝子変異陽性の遠隔移転を有する去勢抵抗性前立線癌、BRCA遺伝子変異陽性の治療切除不能な膵癌における白金系抗悪性腫瘍剤を含む化学療法後の維持療法に対する効能又は効果で承認を取得しております。
参考資料
LYNPARZA®(オラパリブ)、アビラテロンとの併用療法が、
転移性去勢抵抗性前立腺がん(mCRPC)の一次治療において、バイオマーカーのステータスに
かかわらず疾患進行または死亡のリスクをアビラテロンと比較して34%減少
PROpel試験は第3相試験として初めて、mCRPCの一次治療において
PARP阻害剤との併用で画像診断に基づく無増悪生存期間の臨床的有用性を示す
2022年2月14日 ニュージャージー州ケニルワース―AstraZenecaとMerck & Co., Inc., Kenilworth, N.J., U.S.A.(米国とカナダ以外ではMSD)は本日、第3相PROpel試験の良好な結果を発表しました。この試験では、転移性去勢抵抗性前立腺がん(mCRPC)に対する一次治療において、LYNPARZA®とアビラテロン+プレドニゾロンの併用療法により、相同組換え修復(HRR)関連遺伝子変異の有無にかかわらず、標準療法であるアビラテロン+プレドニゾロンのみを投与した場合と比較して、画像診断に基づく無増悪生存期間(rPFS)について、統計学的に有意で臨床的に意味のある改善が示されました。
この試験結果は、2022年米国臨床腫瘍学会(ASCO)の泌尿器がん(GU)シンポジウムで2022年2月17日に発表されます(アブストラクト#11)。
前立腺がんは、男性(出生時の性別として)のがんの中で世界で2番目に多いがんで、2020年には世界で推定140万人が前立腺がんと診断されています。進行前立腺がん患者の約10〜20%が5年以内にCRPCに至ると考えられており、そのうち84%以上がCRPC診断時に転移を有しています。進行前立腺がん患者さんの5年生存率は低く、予後は特に不良です。
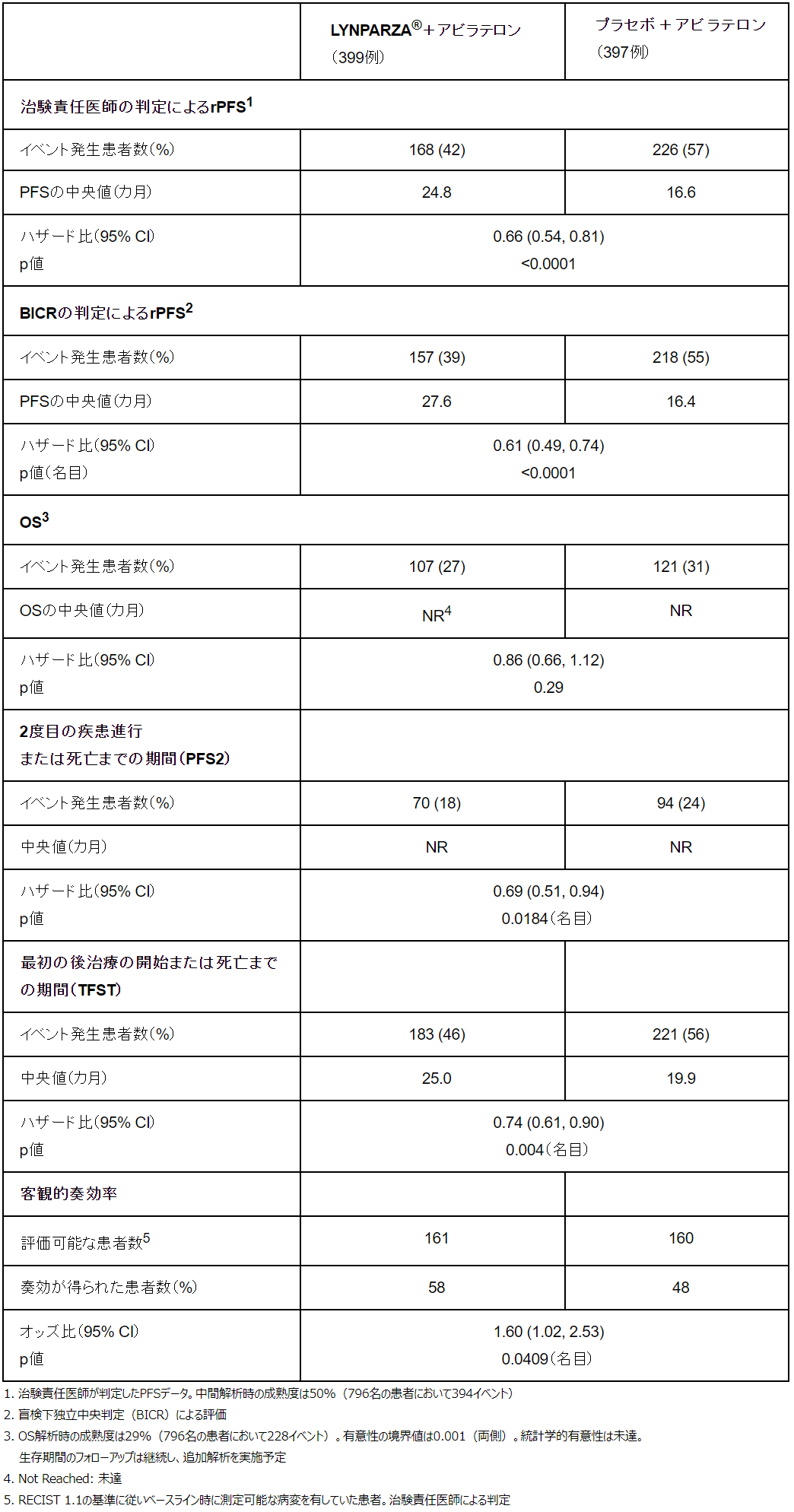
PROpel試験は、無作為化二重盲検多施設共同第3相試験です。2021年9月に実施した、事前に設定した中間解析において、独立データ監視委員会は、PROpel試験において主要評価項目であるrPFSが達成されたと結論づけました。LYNPARZA®とアビラテロン+プレドニゾロンの併用療法(399例)では、mCRPC患者において、HRR関連遺伝子変異の有無にかかわらず、アビラテロン+プレドニゾロンおよびプラセボ(397例)と比較して、疾患進行または死亡のリスクが34%低下しました(HR=0.66 [95% CI, 0.54-0.81]; p<0.0001)。rPFSの中央値はLYNPARZA®とアビラテロンの併用群では24.8カ月、アビラテロンの群では16.6カ月であり、8カ月以上の改善が認められました。
LYNPARZA®+アビラテロンで最も高頻度に認められた有害事象(AE、20%以上)は、貧血(46%)、疲労(37%)、悪心(28%)でした。グレード3以上のAEは、貧血(15%)、高血圧(4%)、尿路感染(2%)、疲労(2%)、食欲減退(1%)、嘔吐(1%)、背部痛(1%)、下痢(1%)、悪心(0.3%)でした。LYNPARZA®とアビラテロンの併用療法群では約14%の患者がAEにより治療を中止しました。探索的評価項目として健康関連QOLを、前立腺がん患者報告アウトカムの尺度であるFACT-P(Functional Assessment of Cancer Therapy-Prostate)を用いて、長期的に評価しました。二群間でQOLの低下は認められませんでした。
またPROpel試験の本中間解析において、LYNPARZA®とアビラテロン+プレドニゾロンの併用療法では、アビラテロン+プレドニゾロンおよびプラセボと比較して、全生存期間(OS)も延長の傾向が認められました。ただしデータカットオフ時における差異は統計学的有意に到達しませんでした(解析時のデータ成熟度は29%、HR=0.86 [95% CI, 0.66-1.12]; p<0.29)。試験では引き続きOSを主な副次評価項目として評価します。
University of Montreal Hospital Centerの泌尿器科責任者で泌尿器がん部門ディレクターであり治験責任医師であるFred Saad教授は、「転移性去勢抵抗性前立腺がんの予後が非常に悪いことは明らかであり、多くの患者さんは有効な治療として一次治療しか受けられません。PROpel試験の結果、オラパリブとアビラテロンの併用療法により、アビラテロンと比較して疾患進行を8カ月以上と大幅に遅らせることが示され、この併用療法が承認されれば、転移性去勢抵抗性前立腺がん患者さんの新たな標準療法の選択肢となる可能性があります」と述べています。
アストラゼネカのエグゼクティブバイスプレジデント兼オンコロジーR&Dの責任者であるSusan Galbraithは、「このLYNPARZA®の併用療法は、一次治療を受ける患者さんのQOLを維持しつつ、疾患進行までの期間を延長する可能性があります。PROpel試験は高いハードルの設定された実薬対照試験であり、LYNPARZA®+アビラテロンが転移性去勢抵抗性前立腺がん患者さんにおいてHRR関連遺伝子変異の有無にかかわらず、現在の標準療法と比較して有意な臨床的改善を示したことは注目に値します」と述べています。
当社研究開発本部のシニアバイスプレジデントでグローバル臨床開発責任者、チーフメディカルオフィサーのRoy Baynes博士は、「PROpel試験の結果、転移性去勢抵抗性前立腺がんの一次治療において、LYNPARZA®とアビラテロン+プレドニゾロンの併用療法により、バイオマーカーのステータスにかかわらず、アビラテロン+プレドニゾロンと比較して、疾患進行または死亡リスクを3分の1低下させることが示されました。この重要な結果を、世界中の保健当局と一日も早く協議していきたいと考えています。この試験に参加している皆様、介護者や医療従事者の皆さんに感謝します」と述べています。
PROpel試験の主な結果
LYNPARZA®は米国ではエンザルタミドまたはアビラテロンによる治療後に進行したHRR関連遺伝子変異を有するmCRPC患者(BRCA遺伝子変異およびその他のHRR関連遺伝子変異)に対する適応が承認されています。欧州連合、日本、中国では、新規ホルモン剤(NHA)を含む治療後に進行したBRCA遺伝子変異陽性のmCRPC患者に対する適応が承認されています。
PROpel試験について
PROpel試験(ClinicalTrials.gov, NCT03732820)は、化学療法またはNHAを一次治療において投与されたことのないmCRPC男性を対象に、アビラテロンに追加投与した場合のLYNPARZA®の有効性、安全性および忍容性をプラセボと比較する多施設共同、無作為化、二重盲検、第3相臨床試験です。また、両治療群の患者には、プレドニゾンまたはプレドニゾロン(1日2回)を投与しました。主要評価項目はrPFSで、副次的評価項目はOS、PFS2およびTFSTです。
この試験では、HRR関連遺伝子変異の有無にかかわらず男性患者を対象としました。前治療として、疾患の前ステージにおけるドセタキセルの治療歴は許容されました。アビラテロンによる治療歴のある患者は対象外でした。無作為化割付け前一年以内に別のNHAによる治療を受けた患者も除外されました。ECOGパフォーマンスステータス(PS)が0または1で、病勢進行が文書で確認され、アビラテロンによる治療に適した患者が対象でした。
LYNPARZA®用法・用量・安全性情報について
用法・用量・安全性情報など一部情報は米国のもので、日本の情報ではありません。詳しくは当社英文リリースをご参照ください。
LYNPARZA ®(olaparib)について
LYNPARZA®はファーストインクラスのPARP阻害剤であり、BRCA遺伝子変異などDNA損傷応答(DDR)経路の異常に作用することで、がん細胞を選択的に死滅させる初の標的治療薬です。LYNPARZA®によるPARP阻害は、DNA一本鎖切断に結合するPARPを捕捉し、複製フォーク停止と崩壊を惹起することで、DNA二本鎖切断を起こしがん細胞を死滅させます。LYNPARZA®はDDR経路に異常をきたした一連のPARP依存性の腫瘍タイプにおいて試験が進行中です。
アストラゼネカとMerck & Co., Inc., Kenilworth, N.J., U.S.A(北米およびカナダ以外ではMSD)が共同で開発と商業化を行っているLYNPARZA®は、広範かつ最先端の臨床試験開発プログラムを有しており、両社は、さまざまながん種にわたり、LYNPARZA®が単剤療法および他の薬剤との併用療法として様々なPARP依存性腫瘍に及ぼす影響を解明するために協業しています。
転移性去勢抵抗性前立腺がん(mCRPC)について
前立腺がんは男性において2番目に罹患率が高いがんで、高い死亡率を伴います。前立腺がんの発症は多くの場合、テストステロンを含むアンドロゲンと呼ばれる男性ホルモンにより促進されます。mCRPCは、アンドロゲンの作用を抑制するアンドロゲン遮断療法を行ったにもかかわらず、前立腺がんが増殖し、他の部位に転移した状態です。進行性前立腺がん患者の約10〜20%が5年以内に去勢抵抗性前立腺がん(CRPC)に至ると考えられており、そのうち84%以上がCRPC診断時に転移を有しています。また、CRPC診断時に転移のない患者のうち33%に、転移が2年以内に発現するとされています。
アストラゼネカとMerck & Co., Inc., Kenilworth, N.J., U.S.A.のがん領域における戦略的提携について
2017年7月、英国アストラゼネカ社とMerck & Co., Inc., Kenilworth, N.J., U.S.A(北米およびカナダ以外ではMSD)は、世界初のPARP阻害剤であるLYNPARZA®を含む特定のがん治療薬について、複数のがん種において共同開発・商業化するがん領域における世界的な戦略的提携を発表しました。両社は、これらの薬剤を他の可能性のある新薬との併用療法および単剤療法として共同開発します。なお、これらのがん治療薬と、各々の会社が保有するPD-L1またはPD-1阻害薬との併用療法は各々の会社で開発します。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.のがん領域における取り組み
Merck & Co., Inc., Kenilworth, N.J., U.S.A.では、画期的な科学を革新的ながん治療薬に変換して世界中のがん患者さんを助けることに取り組んでいます。当社のオンコロジー事業にとって、がんと闘う人々を助けることは私たちの情熱であり、がん治療薬へアクセスしやすくすることは私たちの責任です。また、がん領域における取り組みの一環として、医薬品業界で一二を争う急成長を遂げている開発プログラムにより、30種類以上のがんに対するがん免疫療法の可能性を模索しています。また、引き続き戦略的買収を通じてポートフォリオを強化し、進行がんの治療を改善する可能性をもつ有望ながん治療薬候補の開発を最優先に進めています。当社のオンコロジー臨床試験について詳しくは、当社ウェブサイトをご覧ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.について
Merck & Co., Inc., Kenilworth, N.J., U.S.A.(米国とカナダ以外ではMSD)は130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。また、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続け、世界最高の研究開発型バイオ医薬品企業を目指しています。詳細については、当社ウェブサイトやTwitter、Facebook、Instagram、YouTube、LinkedInをご参照ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.の将来に関する記述
このニュースリリースには、米国の1995年私的証券訴訟改革法(the Private Securities Litigation Reform Act of 1995)の免責条項で定義された「将来に関する記述」が含まれています。これらの記述は、Merck & Co., Inc., Kenilworth, N.J., U.S.A.の経営陣の現時点での信条と期待に基づくもので、相当のリスクと不確実性が含まれています。新薬パイプラインに対する承認取得またはその製品化による収益を保証するものではありません。予測が正確性に欠けていた場合またはリスクもしくは不確実性が現実化した場合、実際の成果が、将来に関する記述で述べたものと異なる場合も生じます。
リスクと不確実性には、業界の一般的な状況および競争環境、金利および為替レートの変動などの一般的な経済要因、昨今の新型コロナウイルス感染症(COVID-19)の世界的大流行の影響、医薬品業界の規制やヘルスケア関連の米国法および国際法が及ぼす影響、ヘルスケア費用抑制の世界的な傾向、競合他社による技術的進歩や新製品開発および特許取得、承認申請などの新薬開発特有の問題、Merck & Co., Inc., Kenilworth, N.J., U.S.A.による将来の市況予測の正確性、製造上の問題または遅延、国際経済および政府の信用リスクなどの金融不安、画期的製品に対するMerck & Co., Inc., Kenilworth, N.J., U.S.A.の特許権やその他の保護の有効性への依存、特許訴訟や規制措置の対象となる可能性等がありますが、これらに限定されるものではありません。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.は、新たな情報、新たな出来事、その他いかなる状況が加わった場合でも、将来に関する記述の更新を行う義務は負いません。将来に関する記述の記載と大きく異なる成果を招くおそれがあるこの他の要因については、Merck & Co., Inc., Kenilworth, N.J., U.S.A.に関するForm 10-Kの2020年度年次報告書および米国証券取引委員会(SEC)のインターネットサイト(www.sec.gov)で入手できるSECに対するその他の書類で確認できます。
# # #
MSDについて
MSD(Merck & Co., Inc., Kenilworth, N.J., U.S.A.が米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。MSDはまた、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続けています。MSDは世界最高の研究開発型バイオ医薬品企業を目指しています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)や Facebook、Twitter、YouTube をご参照ください。