Merck & Co., Inc., Rahway, N.J., USA 2023年度第3四半期決算発表
2023/11/30 13:00 JST
報道関係各位
MSD株式会社
この参考資料は、Merck & Co., Inc., Rahway, N.J., USAが2023年10月26日付(米国東部時間)で発表した2023年度第3四半期決算のプレスリリースMerck Announces Third-Quarter 2023 Financial Resultsを日本語に翻訳したもので、内容および解釈については英語が優先されます。
以下の医療用医薬品は、日本国内で発売しております。カナ表記は括弧内をご参考ください。 BRIDION®(ブリディオン®)、GARDASIL®(ガーダシル®)、GARDASIL®9(日本ではシルガード®9)、JANUVIA®(ジャヌビア®)、KEYTRUDA®(キイトルーダ®)、LAGEVRIO®(ラゲブリオ®)、Lenvima®(レンビマ®)、Lynparza®(リムパーザ®)、 PNEUMOVAX ®23(ニューモバックス®NP)、PREVYMIS®(プレバイミス®)、VAXNEUVANCE®(バクニュバンス®)
参考資料
Merck & Co., Inc., Rahway, N.J., USA
2023年度第3四半期決算発表
- オンコロジーおよびワクチン領域における持続的な成長を反映
- 2023年度第3四半期の全世界売上高は、前年同期比7%増の160億ドル。LAGEVRIOの売上を除き6%増の成長。LAGEVRIOの売上および為替変動の影響を除き8%増の成長
- KEYTRUDAの売上高は、17%の成長で63億ドル(為替の影響を除き17%増)
- GARDASILおよびGARDASIL 9の売上高は、13%の成長で26億ドル(為替の影響を除き16%増)
- LAGEVRIOの売上高は、47%の成長で6億4,000万ドル(為替の影響を除き51%増)
- 2023年度第3四半期のGAAPベースのEPSは1.86ドル、non-GAAPベースでは2.13ドル
- 臨床開発ステージにある3つの抗体薬物複合体(ADC)に関して第一三共との提携契約を発表
- KEYNOTE-671試験に基づき、特定の非小細胞肺がん(NSCLC)患者に対する化学療法を併用した周術期療法としてFDAからKEYTRUDAの承認を取得
- Sotaterceptに関する生物製剤承認申請をFDAが優先審査に指定
- 2023年欧州臨床腫瘍学会(ESMO)年次総会において、以下の有望な新規データを発表:
- 第3相KEYNOTE-671試験のデータ
- Seagenおよびアステラス製薬との提携のもとで実施した第3相KEYNOTE-A39/EV-302試験のデータ
- オンコロジー、心血管代謝および免疫領域を含む複数の治療分野にて2023年に第3相試験を開始
- 2023年度通期の業績見通し
- 2023年度通期の全世界売上高を597億ドル~602億ドルに上方修正(為替のマイナス影響約2%ポイントを含む。業績見通しには、LAGEVRIOの売上約13億ドルを含む)
- 現在、2023年度通期のnon-GAAPベースのEPSレンジを1.33ドル~1.38ドルと予想(為替のマイナス影響約6%ポイントを含む。業績見通しには、第一三共との提携契約に関連する一時金55億ドル、一株当たり1.70ドルによるマイナス影響を反映)
米国ニュージャージー州ローウェイ– Merck & Co., Inc., Rahway, N.J., USA(米国とカナダ以外ではMSD)は2023年10月26日、2023年度第3四半期決算を発表しました。
会長兼最高経営責任者(CEO)のロバート・M・デイビスは、「今年度第3四半期決算の堅調な業績は、重要なイノベーションをもたらし、ブレイクスルーを追求するという当社の才能あるチームのコミットメントを反映しています。これらは、私たちに期待を寄せているすべての方々のための取り組みです。当社は、継続的にサイエンスの限界を押し広げながら、多様なパイプラインを増強するために規律ある投資を行い、患者さんのニーズに応える革新的な治療法の開発を加速させるべく専門知識を応用しています。これらの一環として、最近、第一三共との提携契約を発表いたしました。私は当社の進捗を誇りに思っており、引き続き、最高のレベルで、現在、そして未来に強力で持続可能な価値を生み出す取り組みを進めてまいります」と述べています。
決算サマリー
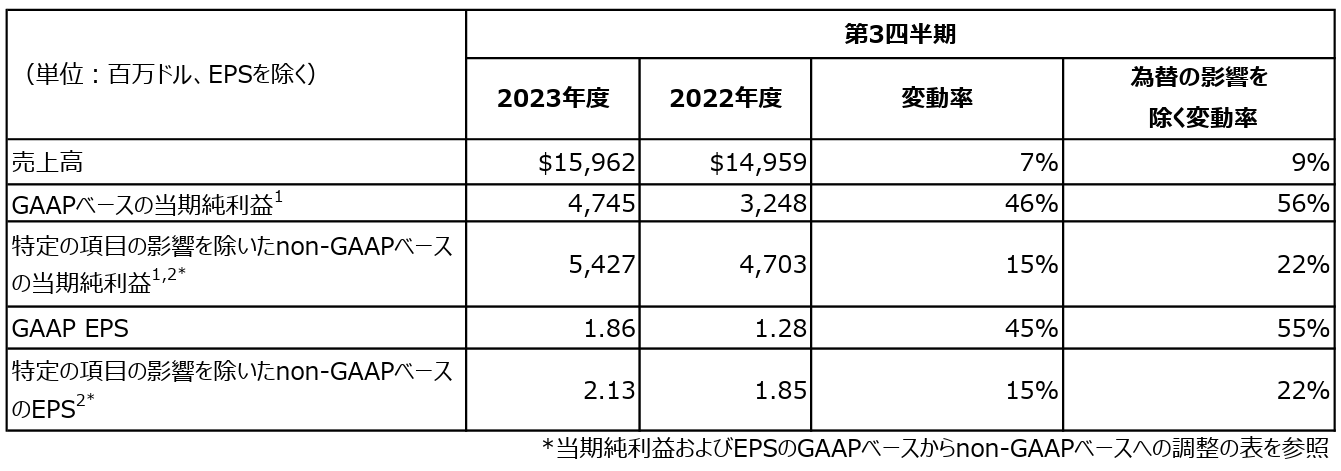
2023年度第3四半期のGAAP(GAAP:一般に公正妥当と認められる会計基準)ベースの希薄化後EPSは1.86ドルでした。2023年度第3四半期のnon-GAAPベースのEPSは2.13ドルでした。2023年度第3四半期のGAAP およびnon-GAAPベースのEPSの前年からの増加は主に、事業面の強み、ならびに2022年に計上したModerna, Inc.(Moderna社)、Orna Therapeutics(Orna社)およびOrion Corporation(Orion社)との提携およびライセンス契約に関連する費用として0.22ドルを反映しています。また2023年度第3四半期のGAAPベースのEPSの増加は、2022年に計上した無形資産の減損損失(2023年は計上せず)、2023年の株式の投資による損失の減少を反映しています。2023年度第3四半期のGAAP およびnon-GAAPベースのEPSの増加は、為替のマイナス影響により一部相殺されました。
non-GAAPベースのEPSは、事業統合・売却関連費用、事業再構築プログラムに関連する費用、および株式の投資による収益と損失を除外しています。
2023年度の第三四半期までの累計の決算数値は、添付の表に記載しています。
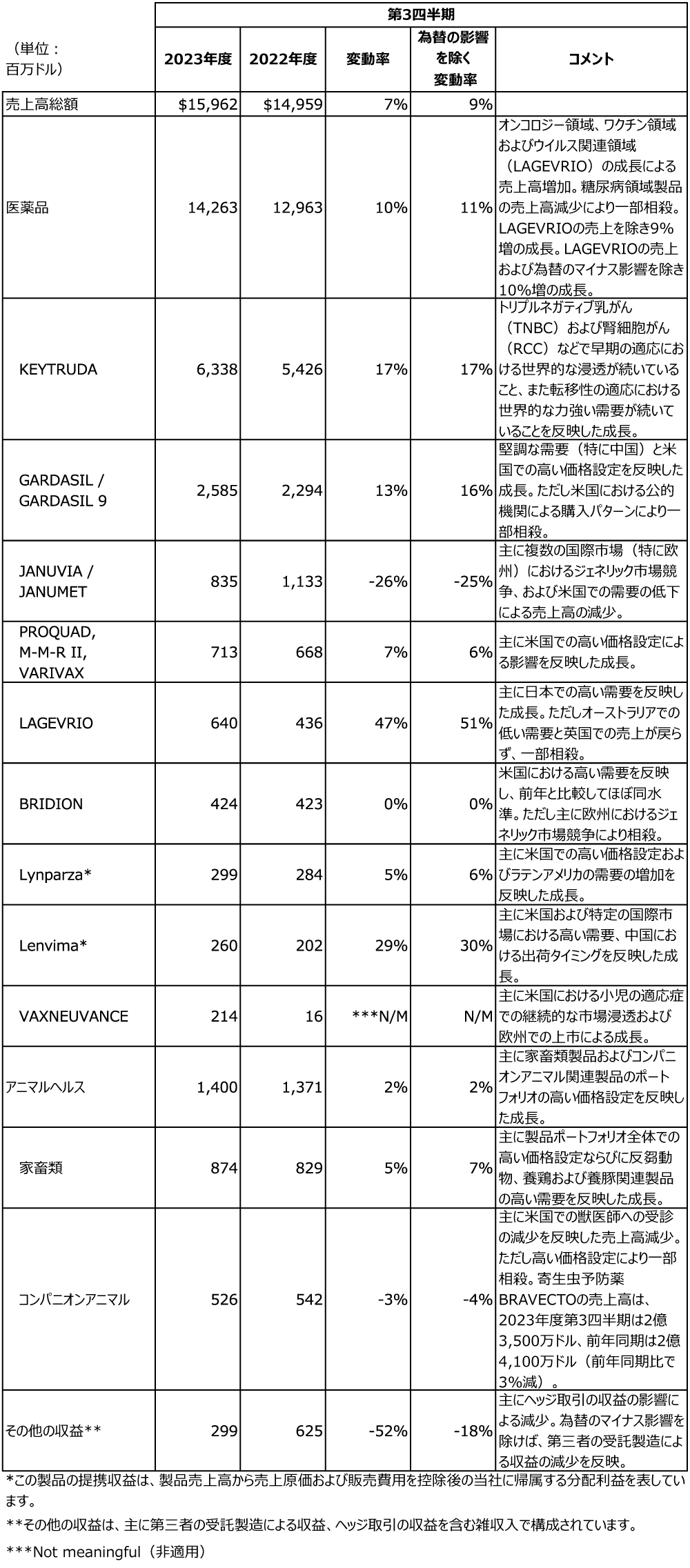
2023年度第3四半期の業績
以下の表は当社の売上高上位製品および主要な製品の売上高総額を表しています。
2023年度第3四半期の費用、EPSおよび関連情報
以下の表は、費用に関する抜粋情報を表しています。
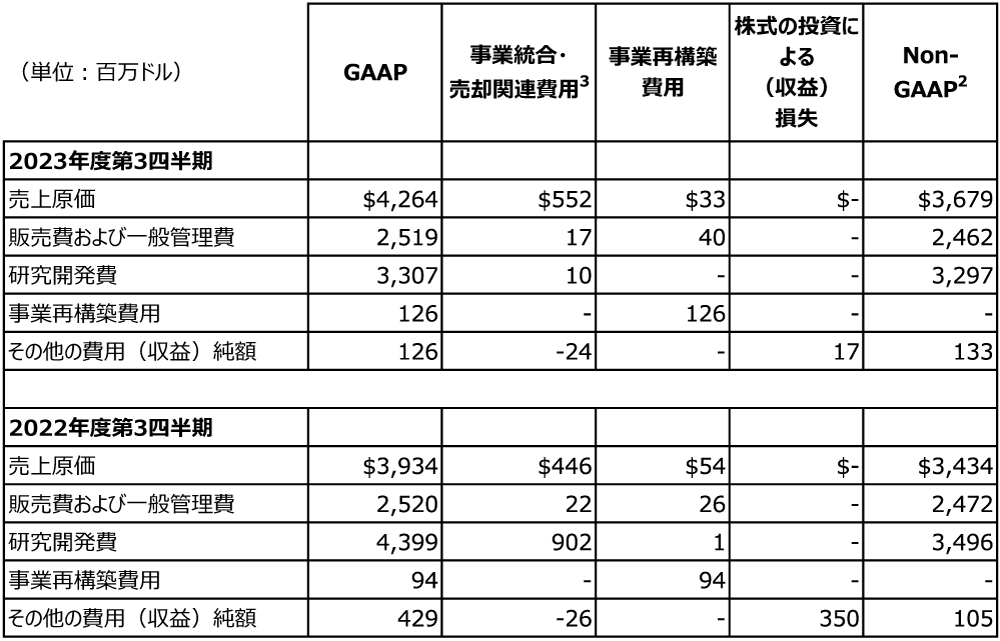
GAAPベースの費用、EPSおよび関連情報
GAAPベースでは、2023年度第3四半期の売上高総利益率は73.3%で、2022年度第3四半期は73.7%でした。この減少は主に、為替のマイナス影響、売上高総利益率が低いLAGEVRIOの売上高増加、および事業統合・売却関連費用の増加を反映しています。この売上高総利益率の減少は、第三者の受託製造による収益の減少、製造関連費用の減少およびプロダクト・ミックスのプラス影響により一部相殺されました。
2023年度第3四半期と2022年度第3四半期の販売費および一般管理費はともに25億ドルでした。これは主に販売促進費の増加を反映していますが、管理費の減少により一部相殺されました。
2023年度第3四半期の研究開発費は33億ドルで、2022年度第3四半期では44億ドルでした。この減少は主に、2022年に計上した無形資産の減損損失8億8,700万ドル(主にnemtabrutinib関連)、ならびにModerna社、Orna社およびOrion社との提携およびライセンス契約に関連する費用6億9,000万ドルを反映しています。この研究開発費の減少は、2023年の報酬および福利厚生費用の増加(人員の増加を一部反映)、開発候補品の発見と初期の医薬品開発への投資の増加、ならびに臨床開発費の増加により一部相殺されました。
2023年度第3四半期のその他の費用(収益)純額は、2022年度第3四半期の4億2,900万ドルの費用に対し1億2,600万ドルの費用を計上しました。これは主に、株式の投資による損失の減少を反映しています。
2023年度第3四半期の実効税率は15.5%で、2022年度第3四半期の実効税率は9.2%でした。
2023年度第3四半期のGAAPベースのEPSは1.86ドル、2022年度第3四半期では1.28ドルでした。
non-GAAPベースの費用、EPSおよび関連情報
non-GAAPベースの売上高総利益率は、2023年度第3四半期と2022年度第3四半期ともに77.0%でした。これは主に、為替のマイナス影響、売上高総利益率が低いLAGEVRIOの売上高増加を反映していますが、第三者の受託製造による収益の減少、製造関連費用の減少およびプロダクト・ミックスのプラス影響により一部相殺されました。
2023年度第3四半期と2022年度第3四半期のnon-GAAPベースの販売費および一般管理費はともに25億ドルでした。これは主に販売促進費の増加を反映していますが、管理費の減少により一部相殺されました。
2023年度第3四半期のnon-GAAPベースの研究開発費は33億ドルで、2022年度第3四半期では35億ドルでした。この減少は主に、2022年に計上したModerna社、Orna社およびOrion社との提携およびライセンス契約に関連する費用6億9,000万ドルを反映しています。この研究開発費の減少は、2023年の報酬および福利厚生費用の増加(人員の増加を一部反映)、開発候補品の発見と初期の医薬品開発への投資の増加、ならびに臨床開発費の増加により一部相殺されました。
non-GAAPベースでの2023年度第3四半期のその他の費用(収益)純額は、2022年度第3四半期の1億500万ドルの費用に対し1億3,300万ドルの費用を計上しました。
2023年度第3四半期のnon-GAAPベースの実効税率は15.0%で、2022年度第3四半期の実効税率は13.6%でした。
2023年度第3四半期のnon-GAAPベースのEPSは2.13ドル、2022年度第3四半期では1.85ドルでした。
当期純利益およびEPSのGAAPベースからnon-GAAPベースへの調整は、以下の表のとおりです。
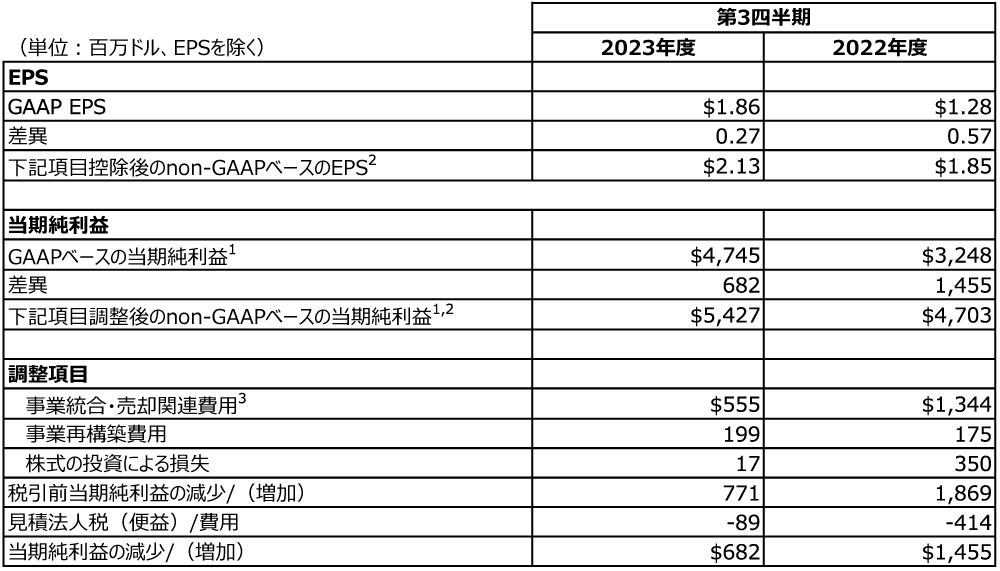
パイプラインおよびポートフォリオハイライト
当社は引き続き、幅広いパイプラインおよびポートフォリオにおいて承認申請と臨床開発のマイルストーンを達成しました。オンコロジー、心血管代謝および免疫領域を含む複数の治療分野と新規の治療モダリティにて2023年に第3相試験を開始しました。これらには、オンコロジー領域として、開発中の個別化ネオアンチゲン療法であるV940とKEYTRUDAの併用療法、抗体薬物複合体(ADC)のMK-2870およびリジン特異的脱メチル化酵素-1阻害候補薬のMK-3543、心血管領域としてはプロタンパク質転換酵素サブチリシン/ケキシン9型(PCSK9)阻害候補薬(経口)のMK-0616、免疫領域としてはヒト化モノクローナル抗体のMK-7240が含まれます。
オンコロジー領域では、早期がんにおけるKEYTRUDAの8番目の承認として、切除可能な非小細胞肺がん(NSCLC)を有する特定の患者さんに対する術前/術後補助療法としてのKEYTRUDAの承認を米国食品医薬品局(FDA)より取得しました。FDAはまた、進行RCCで治療歴を有する特定の患者さんを対象としたWELIREG、子宮頸がん患者さんを対象としたKEYTRUDAの2件の適応追加申請(sNDA)を優先審査項目に指定しました。特に、2023年欧州臨床腫瘍学会(ESMO)年次総会において、当社は有望な新規データを発表し、早期がんにおける当社の進展、転移疾患における基本的ポジション、および多様なオンコロジーパイプラインにおける持続的な進展を紹介しました。
心血管領域では、肺動脈性肺高血圧症(PAH、WHO Group 1)の成人患者さんを対象とした第3相STELLAR試験による臨床的に意義のある結果に基づき、開発中の新規アクチビンシグナル伝達阻害剤のsotaterceptに関する新規の生物製剤承認申請(BLA)をFDAが優先審査に指定しました。FDAは、処方薬ユーザーフィー法(PDUFA)の審査完了予定日を2024年3月26日に設定しました。sotaterceptが承認されれば、このクラスでは初の薬剤となり、肺動脈に関連する希少かつ進行性の疾患に対処することができる新たなアプローチをもたらします。当社は欧州連合(EU)の欧州医薬品委員会(CHMP)への申請も完了しました。
さらに当社は、複数の固形がんを対象とした単独療法および/または他剤との併用療法による治療薬として臨床開発ステージにある、3つのファーストインクラスのDXd ADCに関して第一三共との提携契約を締結しました。この第一三共との提携契約は、当社のオンコロジーパイプラインをさらに加速させ、多様性をもたらします。
以下の表は、当社のパイプラインおよびポートフォリオに関する重要な最新ニュースリリースを表しています。
オンコロジー
| 第3相KEYNOTE-671試験の結果に基づき、切除可能な(T≥4 cmまたはN+)NSCLC患者を対象としたKEYTRUDAと化学療法との併用による術前補助療法と、それに続くKEYTRUDA単独の術後補助療法をFDAが承認 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-A18試験の結果に基づき、新たに高リスクの局所進行子宮頸がんと診断された患者を対象としたKEYTRUDAと同時化学放射線療法の併用療法をFDAが優先審査項目に指定。FDAは、PDUFAよる期日を2024年1月20日に指定 | プレスリリース(英文)はこちら |
| 第3相LITESPARK-005試験の結果に基づき、前治療歴のある進行RCC患者を対象としたWELIREGのsNDAをFDAが優先審査項目に指定。FDAは、PDUFAよる期日を2024年1月17日に指定 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-091試験の結果に基づき、再発リスクが高いNSCLCの成人患者に対する完全切除およびプラチナ製剤ベース化学療法後の術後補助療法としてKEYTRUDAを欧州委員会(EC)が承認 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-811試験の結果に基づき、PD-L1を発現(CPS≧1)した、HER2陽性の進行胃腺がんまたは食道胃接合部(GEJ)腺がんに対する一次治療として、KEYTRUDAとトラスツズマブおよび化学療法との併用療法をECが承認 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-859試験の結果に基づき、PD-L1を発現(CPS≧1)した、HER2陰性の進行胃腺がんまたはGEJ腺がんに対する一次治療としてのKEYTRUDAと化学療法との併用療法について、EUがCHMPの肯定的な見解を採択 | プレスリリース(英文)はこちら |
| 第3相PROpel試験の結果に基づき、BRCA遺伝子変異陽性の遠隔転移を有する去勢抵抗性前立腺がんの治療としてリムパーザとアビラテロンおよびプレドニゾロンの併用療法を日本の厚生労働省が承認 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-671試験の結果に基づき、II期、IIIA期、IIIB期の切除可能なNSCLCに対して、術前のKEYTRUDAと化学療法との併用療法と、それに続く術後のKEYTRUDA単独療法が、術前の化学療法と比較して死亡リスクを28%低下 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-A39/EV-302試験の結果に基づき、治療歴がなく局所進行性または転移性尿路上皮がん患者を対象としたKEYTRUDAとPadcevの併用療法が、化学療法と比較して死亡リスクを50%超低下 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-A18試験の結果に基づき、新たに高リスク局所進行子宮頸がんと診断された患者を対象に、KEYTRUDAと同時化学放射線療法の併用療法が、同時化学放射線療法単独と比較して無増悪生存期間(PFS)の有意な改善を達成 | プレスリリース(英文)はこちら |
| 第3相LITESPARK-005試験の結果に基づき、前治療歴のある進行RCC患者を対象として、WELIREGがエベロリムスと比較してPFSおよび客観的奏効率を有意に改善 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-756試験の結果に基づき、ハイリスクで早期のER+/HER2-乳がんに対する術前薬物療法において、KEYTRUDAと化学療法との併用療法が化学療法単独と比較して病理学的完全奏効率を統計学的に有意に改善 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-811試験の結果に基づき、HER2陽性の進行胃腺がんまたはGEJ腺がんに対する一次治療において、KEYTRUDAとトラスツズマブおよび化学療法との併用療法がPFSを有意に改善 | プレスリリース(英文)はこちら |
| 第3相KEYNOTE-123試験の結果に基づき、術後の筋層浸潤性尿路上皮がん患者を対象として、KEYTRUDAが無病生存期間を有意に改善 | プレスリリース(英文)はこちら |
心血管系
| 第3相STELLAR試験の結果に基づき、PAHの成人患者を対象とした、新規アクチビンシグナル伝達阻害剤のsotaterceptに関する新規のBLAをFDAが優先審査に指定。FDAは、PDUFAよる期日を2024年3月26日に指定 | プレスリリース(英文)はこちら |
| 第3相STELLAR試験およびSOTERIA試験の結果に基づき、PAHの成人患者を対象とした、開発中のsotaterceptに関する有望な最新の解析結果を発表 | プレスリリース(英文)はこちら |
| PCSK9阻害候補薬(経口)のMK-0616に関する第3相臨床プログラムを開始 | プレスリリース(英文)はこちら |
ワクチン
| GARDASILの持続的な免疫原性と安全性に関する長期フォローアップ試験のデータを医学雑誌Pediatricsで公表 | プレスリリース(英文)はこちら |
病院急性期
| 第3相P002試験およびP040試験の結果に基づき、PREVYMISについて、高リスクの腎臓移植レシピエントの成人患者におけるサイトメガロウイルス(CMV)疾患の予防、また晩期CMV感染および疾患のリスクを有する造血幹細胞移植レシピエントの成人患者における200日間延長投与について、EU のCHMPが肯定的な見解を採択 | プレスリリース(英文)はこちら |
サステナビリティハイライト
私たちは、サステナビリティに関する取り組みの成果をまとめた「2022/2023インパクトレポート」を発行しました。これは、医療アクセスの向上と責任ある経営のコミットメントに向けた力強い前進を反映するものです。このインパクトレポートでは、2022年に世界の5億人以上の人々に対して、どのように当社のイノベーションを届けたのか、さらに2025年の医療アクセスに関する目標のうち2項目の目標を引き上げたことに言及しています。
2023年通期の業績見通し
以下の表は、当社の2023年通期の業績見通しの要約を表しています。
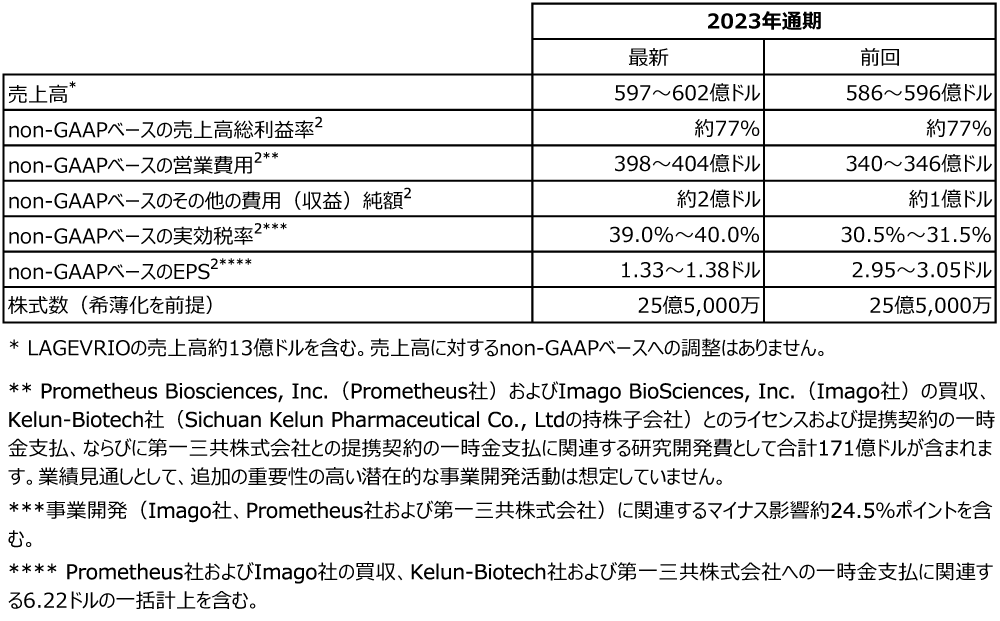
将来の見通しとしてのnon-GAAPベースの売上高総利益率、non-GAAPベースの営業費用、non-GAAPベースのその他の費用(収益)純額、non-GAAPベースの実効税率、およびnon-GAAPベースのEPSに関して、最も直接的な比較を可能とするGAAPベースの指標への調整は提示していません。このような調整には、無形資産の減損損失、法的なセトルメント、株式の投資による利益/損失(直接的な保有または投資ファンドによる所有権)などを含みますが、合理的な確実性をもとに調整金額を予測することができないからです(非合理的な取り組みは除く)。これらの項目は、本質的に予測が困難であり、当社における将来のGAAPベースの業績に重大な影響を及ぼす可能性があります。
当社は、オンコロジーおよびワクチン領域において主要な成長製品の世界的に堅調な需要を取り込み続けています。そのため通期の業績見通しを上方修正しました。当社は、2023年10月中旬の為替を基準として、為替のマイナス影響約2%ポイントを含み、2023年度通期の売上高を597億ドル~602億ドルになると予想しています。2023年通期の業績見通しには、LAGEVRIOの売上高約13億ドルが引き続き含まれます。
2023年度通期のnon-GAAPベースの実効税率は、39.0%~40.0%になると予想しています(事業開発活動に関連するマイナス影響約24.5%ポイントを含む)。
当社は、2023年10月中旬の為替を基準として、為替のマイナス影響約6%ポイントを含み、2023年度通期のnon-GAAPベースのEPSレンジを$1.33ドル~1.38ドルになると予想しています。このnon-GAAPベースのEPSレンジの見直しは、以下の項目を反映しています(過去の業績見通しには反映していません):
- 事業のさらなる堅調性(一株当たり約0.15ドル)
- 第一三共との提携契約に関連する税引前費用55億ドル、一株当たり1.70ドル
- 第一三共とのADCアセットの開発推進費用および取引への出資関連費用として2023年度第4四半期に一株当たり約0.04ドルを予想
- 為替のマイナス影響の 1%増大(一株当たり約0.05ドル)
non-GAAPのEPSレンジでは、事業統合・売却関連費用、事業再構築プログラムに関連する費用、および株式の投資による収益と損失、Zetiaの反トラスト訴訟の特定の原告との和解に関連する費用(以前に発表済)を除外しています。
コンファレンス・コール
Merck & Co., Inc., Rahway, N.J., USAの投資家、メディア関係者および一般の方々へのコンファレンス・コールのライブ・ウェブキャストがで米国東部時間の2023年10月26日木曜日の午前9時に行われました。売上高と利益のニュースリリース、財務状況の開示追補、事前準備所見、決算ハイライトスライドを含むウェブキャストは、www.merck.comにてご覧いただくことができます。
すべての参加者は、(888) 769-8514(フリーダイヤル、米国およびカナダ)または(517) 308-9208からアクセスコード番号8206435にてご参加いただけます。
Merck & Co., Inc., Rahway, N.J., USAについて
Merck & Co., Inc., Rahway, N.J., USA(米国とカナダ以外ではMSD)は、最先端のサイエンスを駆使して、世界中の人々の生命を救い、生活を改善するというパーパスのもとに結束しています。130年以上にわたり、重要な医薬品やワクチンの発見を通して人類に希望をもたらしてきました。私たちは、世界トップクラスの研究開発型バイオ医薬品企業を目指し、人類や動物の疾患予防や治療に寄与する革新的なヘルスケア・ソリューションを提供するために、研究開発の最前線で活動しています。私たちは、多様かつ包括的な職場環境を醸成し、世界中の人々と地域社会に、安全で持続可能かつ健康な未来をもたらすため、責任ある経営を日々続けています。詳細については、当社ウェブサイトやTwitter、Facebook、YouTube、LinkedInをご参照ください。
Merck & Co., Inc., Rahway, N.J., USAの将来に関する記述
このニュースリリースには、米国の1995年私的証券訴訟改革法(the Private Securities Litigation Reform Act of 1995)の免責条項で定義された「将来に関する記述」が含まれています。これらの記述は、Merck & Co., Inc., Rahway, N.J., USAの経営陣の現時点での信条と期待に基づくもので、相当のリスクと不確実性が含まれています。新薬パイプラインに対する承認取得またはその製品化による収益を保証するものではありません。予測が正確性に欠けていた場合またはリスクもしくは不確実性が現実化した場合、実際の成果が、将来に関する記述で述べたものと異なる場合も生じます。
リスクと不確実性には、業界の一般的な状況および競争環境、金利および為替レートの変動などの一般的な経済要因、昨今の新型コロナウイルス感染症(COVID-19)の世界的大流行の影響、米国および世界における医薬品業界の規制やヘルスケア関連の法制度が及ぼす影響、ヘルスケア費用抑制の世界的な傾向、競合他社による技術的進歩や新製品開発および特許取得、承認申請などの新薬開発特有の問題、Merck & Co., Inc., Rahway, N.J., USAによる将来の市況予測の正確性、製造上の問題または遅延、国際経済および政府の信用リスクなどの金融不安、革新的製品に対するMerck & Co., Inc., Rahway, N.J., USAの特許権やその他の保護の有効性への依存、特許訴訟や規制措置の対象となる可能性等がありますが、これらに限定されるものではありません。
Merck & Co., Inc., Rahway, N.J., USAは、新たな情報、新たな出来事、その他いかなる状況が加わった場合でも、将来に関する記述の更新を行う義務は負いません。将来に関する記述の記載と大きく異なる成果を招くおそれがあるこの他の要因については、Merck & Co., Inc., Rahway, N.J., USAに関するForm 10-Kの2022年度年次報告書および米国証券取引委員会(SEC)のインターネットサイト(www.sec.gov)で入手できるSECに対するその他の書類で確認できます。
補足資料
製品名と有効成分を以下に提示します。
医薬品
BRIDION (スガマデクス)
GARDASIL (組換え沈降4価 [6、11、16、18型] ヒトパピローマウイルス様粒子ワクチン)
GARDASIL 9 (組換え沈降9価ヒトパピローマウイルス様粒子ワクチン)
JANUMET (シタグリプチン/メトホルミン)
JANUVIA (シタグリプチン)
KEYTRUDA (ペムブロリズマブ)
LAGEVRIO (モルヌピラビル)
Lenvima (レンバチニブ)
Lynparza (オラパリブ)
M-M-R II (麻しん-おたふくかぜ-風しん混合ワクチン)
PREVYMIS (レテルモビル)
PROQUAD(麻しん-おたふくかぜ-風しん-水痘混合ワクチン)
VARIVAX (水痘ワクチン)
VAXNEUVANCE (15価肺炎球菌結合型ワクチン)
WELIREG (ベルズチファン)
アニマルヘルス
BRAVECTO (フルララネル)
1 Merck & Co., Inc., Rahway, N.J., USAに帰属する当期純利益(損失)。
2 Merck & Co., Inc., Rahway, N.J., USAは、特定項目の性質およびそれらが事業業績や傾向に関する分析に与える影響を考慮し、2023年度および2022年度の特定の項目の影響を除いたnon-GAAPベースの情報を提供しています。経営陣は、non-GAAPベースの決算報告を用いて業績を評価しているため、この情報が会社の業績に対する投資家の理解を深めるものと考えています。経営陣は、non-GAAPベースの指標を目標の設定や達成予測のため、またその他の基準も併用しながら当社の業績を評価するために社内的に活用します。加えて、上級管理職の年間報酬は部分的にnon-GAAPベースの税引前利益をベースとして支払われています。これはGAAPに基づき算出された情報に関する追加情報であって、その代わりとなるものではなく、また優先されるものでもありません。non-GAAPベースの調整についての詳細は、本リリースに添付された表2a(脚注を含む)を参照してください。
3 事業統合・売却に関する統合費用、取引費用およびその他の費用、ならびに提携やライセンス契約に関連する無形資産の償却費と共に、買収の結果認識された無形資産の償却費および棚卸資産に対するパーチェス法適用に伴う調整額、無形資産の減損損失、および、条件付対価による負債の公正価値測定の見積り変更に関連する費用または収益が含まれます。2022年度第3四半期の研究開発費の無形資産の減損損失は8億8,700万ドルで、主にnemtabrutinibに関連したものです。
# # #
MSDについて
MSD(Merck & Co., Inc., Rahway, N.J., USAが米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、最先端のサイエンスを駆使して、世界中の人々の生命を救い、生活を改善するというパーパスのもとに結束しています。130年以上にわたり、重要な医薬品やワクチンの発見を通して人類に希望をもたらしてきました。私たちは、世界トップクラスの研究開発型バイオ医薬品企業を目指し、人類や動物の疾患予防や治療に寄与する革新的なヘルスケア・ソリューションを提供するために、研究開発の最前線で活動しています。私たちは、多様かつ包括的な職場環境を醸成し、世界中の人々と地域社会に、安全で持続可能かつ健康な未来をもたらすため、責任ある経営を日々続けています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)やFacebook、Twitter、YouTube、LinkedInをご参照ください。
