Merck & Co., Inc., Kenilworth, N.J., U.S.A. 2021年度第2四半期決算発表
2021/08/17 00:00 JST
報道関係各位
MSD株式会社
この参考資料は、Merck & Co., Inc., Kenilworth, N.J., U.S.A.が2021年7月29日付(米国東部時間)で発表した2021年度第2四半期決算のプレスリリース Merck Announces Second-Quarter 2021 Financial Results を日本語に翻訳したもので、内容および解釈については英語が優先されます。
以下の医療用医薬品は日本国内で発売しております。カナ表記は括弧内をご参考ください。
BRIDION®(ブリディオン®)、GARDASIL®(ガーダシル®)、ISENTRESS®(アイセントレス®)、JANUVIA®(ジャヌビア®)、KEYTRUDA®(キイトルーダ®)、Lenvima®(レンビマ®)、Lynparza®(リムパーザ®)、PREVYMIS®(プレバイミス®)、ROTATEQ®(ロタテック®)
参考資料
Merck & Co., Inc., Kenilworth, N.J., U.S.A.
2021年度第2四半期決算発表
- 2021年度第2四半期の全世界売上高は(Organon社の業績を除外した継続的事業活動に基づく)、前年同期比22%増の114億ドル(為替の影響を除き19%増)。COVID-19パンデミックからの継続的な回復および当社の画期的製品のポートフォリオによる堅調な潜在需要を反映:
- KEYTRUDAの売上高は、23%の成長で42億ドル(為替の影響を除き20%増)
- GARDASIL/GARDASIL 9の売上高は、88%の成長で12億ドル(為替の影響を除き78%増)
- アニマルヘルスの売上高は、34%の成長で15億ドル(為替の影響を除き27%増)
- 2021年度第2四半期のGAAPベースのEPSは0.48ドル(継続的事業活動に基づく)、non-GAAPベースでは1.31ドル(継続的事業活動に基づく)
- パイプラインの進展および複数の承認を取得:成人用の15価肺炎球菌結合型ワクチンであるVAXNEUVANCEについてFDAによる承認、高リスク早期トリプルネガティブ乳がんに術前/術後補助療法としてKEYTRUDAと化学療法の併用療法についてFDAによる承認(KEYNOTE-522試験に基づく)、進行性子宮内膜がんの特定の患者に対するKEYTRUDAとLenvimaの併用療法についてFDAによる承認(KEYNOTE-775試験/ 309試験に基づく)
- 6月2日にOrganon社の分社化が完了し、約90億ドルの分配金を受領
- 2021年業績見通し(継続的事業活動に基づく)
- 2021年度通期の売上高成長を12%~14%と予想。為替のプラス影響約2%未満を含み、2021年度通期の収益を464億ドル~474億ドルに上方修正
- 2021年度通期のGAAPベースのEPSレンジを4.24ドル~4.34ドル、2021年度通期のnon-GAAPベースのEPSレンジを5.47ドル~5.57ドルと予想(為替のプラス影響約2%を含む)
米国ニュージャージー州ケニルワース– Merck & Co., Inc., Kenilworth, N.J., U.S.A.(米国とカナダ以外ではMSD)は2021年7月29日、2021年度第2四半期の決算を発表しました。
会長兼最高経営責任者(CEO)ロバート・M・デイビスは、「当社の業績に対するCOVID-19パンデミックの影響が減少するとともに、当社の主要な成長ドライバーが支える業績基盤の力強い進展が大きな励みとなりました。創薬研究体制の強化と、患者さんへイノベーションを届けるスピード、緊急性、機敏性を向上させることで、私たちは持続的かつ長期的な成長と価値の創出を実現できると確信しています」と述べています。
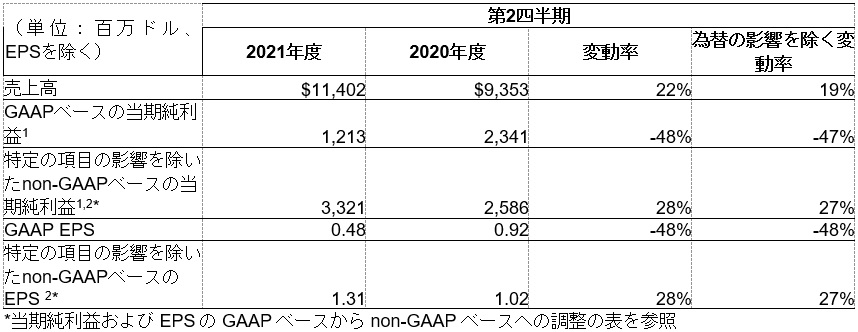
決算サマリー(継続的事業活動に基づく)
Organon & Co.(Organon社)の分社化において、Organon社の業績は現在、非継続的事業活動として計上しています。本リリースで提示される決算情報は、Organon社の業績を除外した継続的事業活動に基づく当社の業績を反映しています。この提示方法に合わせて過去の決算情報を訂正し再提示しています。2021年6月21日、当社は、Organon社の業績を非継続的事業活動として、過去の財務情報を再計算して反映させたForm 8-Kを申請しています。
2021年度第2四半期のGAAP(GAAP:一般に公正妥当と認められる会計基準)ベースの希薄化後EPSは0.48ドルでした。2021年度第2四半期のGAAPベースのEPSは、Pandion Therapeutics(Pandion社)の買収に関連する費用17億ドルを反映しています。2021年度第2四半期のnon-GAAPベースのEPSは1.31ドルで、事業統合・売却関連費用、事業再構築費用、株式の投資による収益と損失、Pandion社の買収に関連する費用、および特定のその他の項目を除外しています。
オンコロジープログラムハイライト
当社は、オンコロジーにおける開発プログラムを引き続き進展させ、2028年までに90種類を超える新規の適応取得を予定しています。この中には、抗PD-1抗体KEYTRUDA(ペムブロリズマブ)、アストラゼネカ社との共同開発・商業化を進める経口ポリADP-リボースポリメラーゼ(PARP)阻害剤Lynparza(オラパリブ)、およびエーザイ社と共同開発・商業化を進める経口チロシンキナーゼ阻害剤Lenvima(レンバチニブメシル酸塩)などが含まれます。
- 主な薬事上の進展は以下のとおりです:
- 第3相KEYNOTE-522試験の結果に基づき、高リスクの早期トリプルネガティブ乳がん(TNBC)患者の治療において、KEYTRUDAと術前化学補助療法との併用療法と、それに続くKEYTRUDAの術後単独補助療法を米国食品医薬品局(FDA)が承認。これら結果は、オンライン開催される欧州臨床腫瘍学会(ESMO)のプレナリーセッションで7月15日に発表。
- 現在進行中の第3相KEYNOTE-811試験の結果に基づき、局所進行性で切除不能または転移性のヒト上皮成長因子受容体 2(HER2)陽性胃腺がんまたは食道胃接合部(GEJ)腺がんに対する一次治療としてKEYTRUDAとトラスツズマブおよび化学療法の併用療法をFDAが承認。これは、上記の患者において、一次治療として抗HER2療法と化学療法との併用で承認された初めての抗PD-1抗体による治療。これは、検証的試験による臨床上の効果の確認を必要とする条件付き迅速承認。
- 第2相KEYNOTE-629試験の結果に基づき、手術または放射線療法による治癒不能な局所進行性の皮膚有棘細胞がん(cSCC)患者に対するKEYTRUDAの単独療法をFDAが承認。
- 検証的ピボタル第3相KEYNOTE-775試験/ 309試験の結果に基づき、全身療法後に増悪した、根治的手術または放射線療法に不適応な高頻度マイクロサテライト不安定性(MSI-H)を有さない、またはミスマッチ修復機能欠損(dMMR)を有さない進行性子宮内膜がんに対するKEYTRUDAと Lenvimaの併用療法をFDAが承認。
- ピボタル第3相CLEAR試験(KEYNOTE-581試験/ 307試験)の結果に基づき、進行性腎細胞がん(RCC)の一次治療としてKEYTRUDAとLenvimaの併用療法をFDAが優先審査に指定。処方薬ユーザーフィー法(PDUFA)に基づく審査終了目標日は8月26日。
- 特定の胃がん患者に対する三次治療としてのKEYTRUDAの迅速承認の維持にFDAの抗がん剤諮問委員会(Oncologic Drugs Advisory Committee)が反対。当社は、プラチナ製剤ベースの化学療法施行中または施行後に病勢進行し、かつ1ライン以上の前治療を受けた再発の局所進行性または転移性の胃腺がんまたは食道胃接合部(GEJ)腺がんに対する治療薬としてのKEYTRUDAの迅速承認の自主的な取り下げを発表。FDAの承諾を得て、当社は2022年1月に取り下げを実行予定。
- 第3相KEYNOTE-590試験に基づき、腫瘍にPD-L1を発現(Combined Positive Score[CPS]≧10)する、局所進行で切除不能または転移性の食道がんまたはHER2陰性GEJ腺がんの成人患者の一次治療としてKEYTRUDAとプラチナ製剤およびフッ化ピリミジン系製剤ベースの化学療法との併用療法を欧州委員会(EC)が承認。
- 第3相PROfound試験のデ-タに基づき、新規ホルモン薬(アビラテロン、エンザルタミド)を含めた前治療後に疾患進行が認められたBRCA遺伝子変異陽性(生殖細胞系/体細胞系)の転移性去勢抵抗性前立腺がんの成人患者に対する単剤療法としてLynparzaを中国国家医薬品管理局(Chinese National Medical Products Administration)が承認。
- 当社は以下の詳細なデータを発表:
- 腫瘍にPD-L1を発現(CPS≧10)する、未治療の転移性のトリプルネガティブ乳がんにKEYTRUDAと化学療法の併用療法を評価する第3相KEYNOTE-355試験で全生存期間(OS)に関する良好なトップラインデータを発表。世界各国の保健当局にデータを提出し、今後の医学学会で発表する予定。
- 特定のRCC患者に対する術後補助療法を検討するピボタル第3相KEYNOTE-564試験の結果を2021年米国臨床腫瘍学会(ASCO)年次総会で発表。この第3相KEYNOTE-564試験において、KEYTRUDAは術後補助療法として、再発または死亡リスクをプラセボと比較して統計学的に有意かつ臨床的に意味のある低減を示す。世界各国の保健当局にデータを提出し、引き続き第3相KEYNOTE-564試験は、重要な副次評価項目であるOSの評価についても継続する予定。
- PD-L1発現の有無にかかわらず、治療抵抗性、再発または転移性子宮頸がん患者に対する一次治療において、KEYTRUDAと化学療法(ベバシズマブ併用または非併用)の併用療法が、OSと無増悪生存期間(PFS)による複合主要評価項目を達成したピボタル第3相KEYNOTE-826試験の結果を発表。この結果は今後の医学学会で発表し、保健当局にデータを提出する予定。
- 当社とアストラゼネカ社は、生殖細胞系列 BRCA1/2変異陽性のHER2陰性早期乳がん患者に対する術後補助療法としてLynparzaが主要評価項目である無浸潤生存期間をプラセボと比較して統計学的に有意に改善した第3相OlympiA試験の初回結果を2021年ASCO年次総会で発表。この結果は世界各国の保健当局に提出し、引き続き第3相OlympiA試験は副次評価項目であるOSの評価についても継続する予定。
ワクチンハイライト
- 肺炎球菌(血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F、33F)による侵襲性感染症の予防のための能動免疫を目的とした、成人用(18歳以上)の15価肺炎球菌結合型ワクチンであるVAXNEUVANCEをFDAが承認したことを発表。
- 50歳以上の成人を対象に、VAXNEUVANCEと13価肺炎球菌結合型ワクチンを比較した、ピボタル第3相PNEU-AGE試験の新規データをEuropean Congress of Clinical Microbiology & Infectious Diseases (ECCMID) 2021にて発表。
- VAXNEUVANCEが、小児を対象とする2件の第3相臨床試験において免疫原性および安全性の主要評価項目を達成したことを発表。小児を対象とする承認追加申請については、今年中にFDAに提出する予定。
HIVハイライト
- HIV-1感染に低リスクの成人に対して、HIV-1感染の曝露前予防投与(PrEP)として当社が開発中のヌクレオシド系逆転写酵素トランスロケーション阻害剤(NRTTI)islatravirの6カ月(24週間)の経口投与による安全性、忍容性および薬物動態をプラセボと比較して評価する第2a相臨床試験の結果を発表。これらは、プラセボと比較して24週間のislatravirのPrEP経口投与レジメンによる安全性プロファイルを裏付ける最新のデータとして11th International AIDS Society Conference on HIV Science(第11回国際エイズ学会)で口頭発表。
その他のハイライト
- 静注療法が必要な代償不全イベントの発生後に安定している、心駆出率が低下した症候性慢性心不全の成人患者に対する治療薬であるVerquvo(vericiguat)について、ECは欧州連合での販売承認を授与。Verquvoはバイエル社と共同開発中。
- 2歳以上の小児患者を対象とした外科手術処置時の筋弛緩薬ロクロニウム臭化物またはベクロニウム臭化物の回復剤であるBRIDION注射液100 mg/mL(スガマデクスナトリウム)をFDAが承認。
- 難治性または原因不明の慢性咳嗽を有する成人患者を対象に、経口治療薬として開発中の選択的P2X3受容体拮抗薬gefapixantに関する新薬承認申請(NDA)の審査期日延長をFDAが決定(申請内容の全文をレビューする時間を確保するため)。PDUFAによる期日を2022年3月21日に延長。
COVID-19ハイライト
- 当社とRidgeback Biotherapeutics LPは、新型コロナウイルス感染症(COVID-19)を引き起こすSARS-CoV-2を含む様々なRNAウイルスの複製を阻害するmolnupiravir(MK-4482)を検討する第2/3相の第2相パートによるトップラインデータを4月に発表。このデータは、7月のECCMIDで発表。molnupiravirは、COVID-19の確定診断を受け、重症化リスク因子を1つ以上有する外来患者の治療薬として、現在第3相MOVe-OUT試験において評価中。
- インドをはじめ、その他の低・中所得国において、各国の規制当局による承認または緊急使用許可を取得後、molnupiravirを速やかに提供できるよう、実績のあるインドのジェネリックメーカー数社とmolnupiravirの非独占的で社会貢献的なライセンス契約を4月に締結したことを発表。
- molnupiravirの調達契約を6月に米国政府と締結したことを発表。
2021年度第2四半期の業績
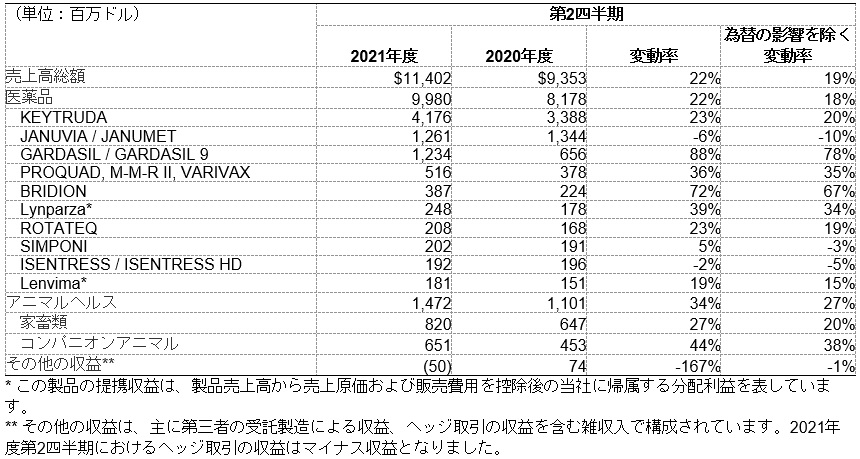
以下の表は当社の医薬品の売上高上位製品およびアニマルヘルス製品の売上高総額を表しています。
医薬品の業績
2021年度第2四半期の医薬品売上高は、22%増の100億ドルとなりました(為替のプラス影響を除き18%増)。この増加は、COVID-19パンデミックからの継続的な回復および堅調な潜在需要を反映しています。このCOVID-19パンデミックは、2021年度第2四半期にマイナス影響を与えましたが、前年同期よりも影響は小さくなりました。COVID-19パンデミックからの回復が前年比売上高成長に与えた正味のプラス効果は、約9億ドルでした。
オンコロジー領域の成長は、主にKEYTRUDAの売上高増加によるもので、KEYTRUDAの当第2四半期の売上高は前年同期比23%増の42億ドルとなっています。KEYTRUDAの世界的な売上高増加は、非小細胞肺がん(NSCLC)の適応における力強い進展が続いていること、また悪性黒色腫の術後補助療法、RCC、膀胱がん、頭頸部扁平上皮がん、MSI-H固形がんを含む継続的な適応症追加を反映しています。さらに、米国、欧州および中国における継続的な適応症の承認を反映し39%の増加となったLynparzaの提携収益、および主に中国における需要の増加を反映し19%増となったLenvimaの提携収益も、オンコロジー領域の売上高増加に貢献しました。
2021年度第2四半期のワクチン領域の成長は、GARDASIL(組換え沈降4価 [6、11、16、18型] ヒトパピローマウイルス様粒子ワクチン)およびGARDASIL 9(組換え沈降9価ヒトパピローマウイルス様粒子ワクチン)の合算売上高の増加が主にけん引しました。2021年度第2四半期のGARDASIL/GARDASIL 9の売上高は、88%増の12億ドルに回復しました。これは、主にCOVID-19パンデミックからの継続的な回復および米国における堅調な潜在需要、および中国などの米国外の継続的な市場の拡大を反映しています。供給量の増加もまたプラス影響となりました。
小児ワクチンであるVARIVAX(水痘ワクチン)、PROQUAD(麻しん-おたふくかぜ-風しん-水痘混合ワクチン)、およびM-M-R II(麻しん-おたふくかぜ-風しん混合ワクチン)の2021年度第2四半期の合算売上高は、米国におけるCOVID-19パンデミックからの継続的な需要回復を主に反映し、36%増の5億1,600万ドルとなりました。
急性期治療・病院領域の成長は、成人および2歳以上の小児患者を対象とした外科手術処置時の筋弛緩薬ロクロニウム臭化物またはベクロニウム臭化物の回復剤であるBRIDION注射液100 mg/mL(スガマデクスナトリウム)の世界的な需要の増加(COVID-19パンデミックからの継続的な回復が一部寄与し、72%増の3億8,700万ドル)、およびサイトメガロウイルス(CMV)抗体陽性の成人の同種造血幹細胞移植患者を対象にしたCMV感染または感染症の予防を目的とする抗ウイルス薬PREVYMIS(レテルモビル)の継続的な市場拡大を反映しています。急性期治療・病院領域の成長は、特定の細菌に感染した成人患者に対する治療薬であるセフェム系抗生物質とベータラクタマーゼ阻害薬の配合剤であるZERBAXA(タゾバクタムナトリウム/セフトロザン硫酸塩)注射剤の2020年度第4四半期の製品回収に伴う一時的な販売停止により、一部相殺されました。
JANUVIA(シタグリプチン)とJANUMET(シタグリプチン/メトホルミン)の当四半期の売上高は、6%減の13億ドルとなりました。これは、米国における継続的な価格抑制の影響を反映していますが、特定の国際市場における需要の増加により一部相殺されました。
アニマルヘルスの業績
アニマルヘルスの2021年度第2四半期の全世界での売上高は、前年同期比で34%増の15億ドルでした(為替のプラス影響を除き、27%増)。アニマルヘルスの売上高増加は、コンパニオンアニマル関連製品の世界的に高い需要(コンパニオンアニマルワクチンがけん引)、およびBRAVECTO(フルララネル)などの寄生虫予防薬の売上高増加を反映しています。家畜類製品の売上高増加は、反芻動物、養豚および養鶏関連製品などの高い需要、およびアニマルヘルスインテリジェンス関連製品の世界的に高い需要を反映しています。このCOVID-19パンデミックは、2020年度第2四半期のアニマルヘルスの売上高にマイナス影響を与えましたが(約1億ドル)、2021年度第2四半期においては影響ありませんでした。
2021年度第2四半期の費用、EPSおよび関連情報
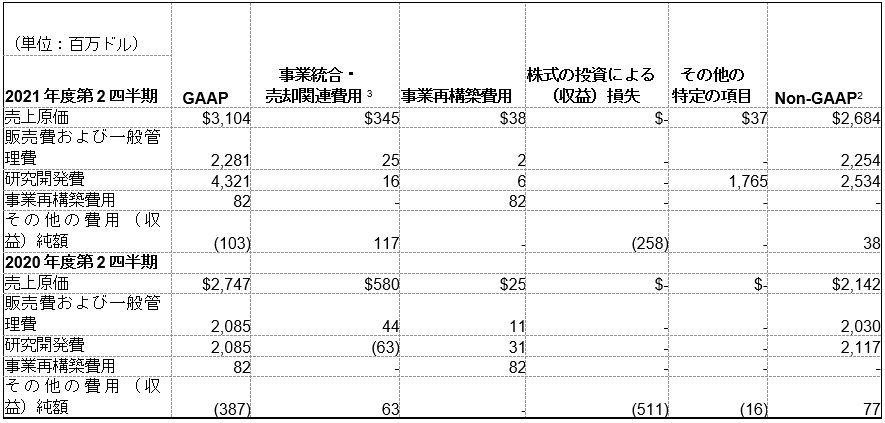
以下の表は、費用に関する抜粋情報を表しています。
GAAPベースの費用、EPSおよび関連情報
GAAPベースでは、2021年度第2四半期の売上高総利益率は72.8%で、2020年度第2四半期では70.6%でした。2021年度第2四半期における売上高総利益率の増加は、事業統合・売却関連費用の減少、およびプロダクト・ミックスのプラス影響によるものですが、為替のマイナス影響、価格抑制および製造コストの増加により一部相殺されました。
2021年度第2四半期の販売費および一般管理費は、前年同期比で9%増の23億ドルでした。この増加は主に、販売促進費および管理費の増加、および為替のマイナス影響を反映しています。
2021年度第2四半期の研究開発費は43億ドルで、2020年度第2四半期は21億ドルでした。この増加は主に、Pandion社の買収に関連する費用17億ドル、臨床開発に関連する費用の増加、および開発候補品の発見と初期の医薬品開発への投資の増加を反映しています。
2021年度第2四半期のその他の費用(収益)純額は、2020度第2四半期の3億8,700万ドルの収益に対し1億300万ドルの収益を計上しました。これは、2020年度と比較して2021年度における株式の投資による収益の減少を主に反映しています。
2021年度第2四半期の実効税率は29.3%となりました。2021年度第2四半期の実効税率は、Pandion社の買収に関連する費用で税務便益が発生しなかったことを反映しています。
2021年度第2四半期のGAAPベースのEPSは0.48ドル、2020年度第2四半期では0.92ドルでした。
non-GAAPベースの費用、EPSおよび関連情報
non-GAAPベースでは、2021年度第2四半期の売上高総利益率は76.5%で、2020年度第2四半期では77.1%でした。2021年度第2四半期のnon-GAAPベースの売上高総利益率の減少は、為替のマイナス影響、価格抑制および製造コストの増加によるものですが、プロダクト・ミックスのプラス影響により一部相殺されました。
2021年度第2四半期のnon-GAAPベースの販売費および一般管理費は、前年同期比で11%増の23億ドルでした。この増加は主に、販売促進費および管理費の増加、および為替のマイナス影響を反映しています。
2021年度第2四半期のnon-GAAPベースの研究開発費は25億ドルで、2020年度第2四半期の20%増となりました。この増加は主に、臨床開発に関連する費用の増加、および開発候補品の発見と初期の医薬品開発への投資の増加を反映しています。
non-GAAPベースでの2021年度第2四半期のその他の費用(収益)純額は、2020年度第2四半期の7,700万ドルの費用に対し3,800万ドルの費用を計上しました。
2021年度第2四半期のnon-GAAPベースの実効税率は14.6%となりました。
2021年度第2四半期のnon-GAAPベースのEPSは1.31ドル、2020年度第2四半期では1.02ドルでした。
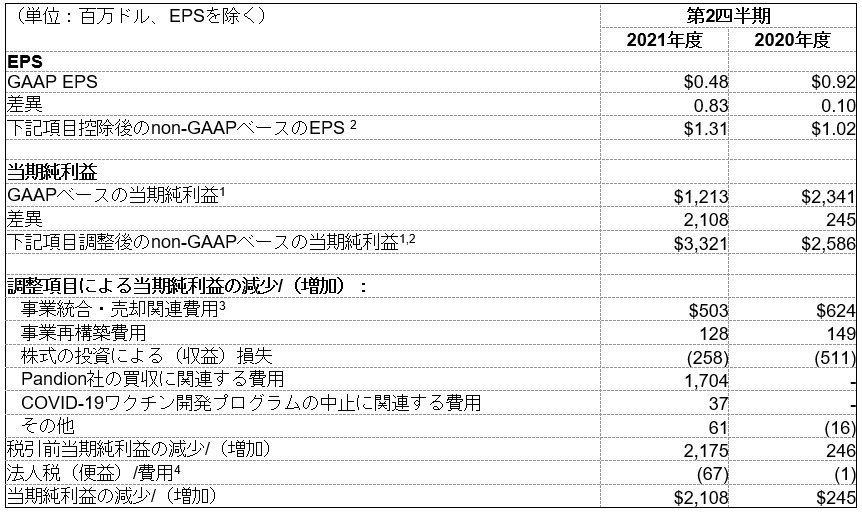
当期純利益およびEPSのGAAPベースからnon-GAAPベースへの調整は、以下の表のとおりです。
業績見通し
当社の事業全体において世界規模で根本的な需要が堅調に続いています。2021年7月中旬の為替を基準として、為替のプラス影響約2%未満を含み、2021年度の売上高成長を12%~14%、2021年度通期の収益を464億ドル~474億ドルになると予想しています。
当社は引き続き、患者さんを含めグローバルな医療システム全体でCOVID-19の影響に対し適応が大きく進んできたと考えており、今後も一定のマイナス影響が残る一方で、回復傾向は継続すると予想しています。当社の2021年度の収益に対して3%未満のCOVID-19パンデミックのマイナス影響が、関連するすべての医薬品セグメントの業績に及ぶと予想しています。
当社は、2021年度通期のGAAPベースのEPSレンジを4.24ドル~4.34ドルと予想しています。
当社は、為替のプラス影響約2%を含み、2021年度通期のnon-GAAPベースのEPSレンジを5.47ドル~5.57ドルと予想しています。このnon-GAAPベースEPSレンジは、事業統合・売却関連費用、事業再構築計画関連費用、株式の投資による収益と損失、および特定のその他の項目を除外しています。
2021年度通期において、当社は引き続き営業費用に対するCOVID-19パンデミックの影響はごくわずかであると予想しています。これは、COVID-19に関する抗ウイルス薬の開発プログラムの費用が、COVID-19パンデミックによりもたらされた他の領域における費用減少のプラス影響を相殺すると予想しているためです。
売上予測またはEPSガイダンスのレンジ予測は、当社のCOVID-19に関する抗ウイルス候補薬molnupiravirが上市する可能性を加味していません。
以下の表は、当社の2021年の業績ガイダンスの要約を表しています。
2021年度のGAAPベースの予想EPSからnon-GAAPベースのEPSへの調整、およびnon-GAAPベースのEPSからの控除項目は以下の表のとおりです。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.について
Merck & Co., Inc., Kenilworth, N.J., U.S.A. (米国とカナダ以外ではMSD)は、130年以上にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。MSDはまた、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続けています。MSDは世界最高の研究開発型バイオ医薬品企業を目指しています。詳細については当社ウェブサイトやMerck & Co., Inc., Kenilworth, N.J., U.S.A.の Twitter 、 Facebook 、 Instagram 、 YouTubeおよび、Linkedlnをご参照ください。
Merck & Co., Inc., Kenilworth, N.J., U.S.A.の将来に関する記述
Merck & Co., Inc., Kenilworth, N.J., U.S.A.(以下、当社)発行のこのニュースリリースには、米国の1995年私的証券訴訟改革法(the Private Securities Litigation Reform Act of 1995)の免責条項で定義された「将来に関する記述」が含まれています。これらの記述は、当社の経営陣の現時点での信条と期待に基づくもので、相当のリスクと不確実性が含まれています。新薬パイプラインに対する承認取得またはその製品化による収益を保証するものではありません。予測が正確性に欠けていた場合またはリスクもしくは不確実性が現実化した場合、実際の成果が、将来に関する記述で述べたものと異なる場合も生じます。
リスクと不確実性には、業界の一般的な状況および競争環境、金利および為替レートの変動などの一般的な経済要因、新型コロナウイルス感染症(COVID-19)の世界的大流行の影響、医薬品業界の規制やヘルスケア関連の米国法および国際法が及ぼす影響、ヘルスケア費用抑制の世界的な傾向、競合他社による技術的進歩や新製品開発および特許取得、承認申請などの新薬開発特有の問題、当社による将来の市況予測の正確性、製造上の問題または遅延、国際経済および政府の信用リスクなどの金融不安、画期的製品に対する当社の特許権やその他の保護の有効性への依存、特許訴訟や規制措置の対象となる可能性等がありますが、これらに限定されるものではありません。
当社は、新たな情報、新たな出来事、その他いかなる状況が加わった場合でも、将来に関する記述の更新を行う義務は負いません。将来に関する記述の記載と大きく異なる成果を招くおそれがあるこの他の要因については、当社に関するForm 10-Kの2020年度年次報告書およびSECのインターネットサイト
(www.sec.gov)で入手できる米国証券取引委員会(SEC)に対するこの他の書類で確認できます。
1 Merck & Co., Inc., Kenilworth, N.J., U.S.A.に帰属する当期純利益
2 Merck & Co., Inc., Kenilworth, N.J., U.S.A.は、事業業績や傾向に関する分析への特定項目の性質による影響を考慮し、2021年度および2020年度の特定の項目の影響を除いたnon-GAAPベースの情報を提供しています。経営陣は、この情報が会社の決算結果および経営陣による業績評価方法に関する投資家の理解を深めるものと考えています。経営陣は、これらの指標を目標の設定や達成予測のため、またその他の基準で当社の業績を評価するために社内的に活用します。加えて、上級管理職の年間報酬の一部はnon-GAAPベースの税引前利益から支払われています。これはGAAPに基づき算出された情報に関する追加情報であって、その代わりとなるものではなく、また優先されるものでもありません。
3 事業統合・売却に関する統合費用、取引費用およびその他の費用と共に、買収の結果認識された無形資産の償却費および棚卸資産に対するパーチェス法適用に伴う調整額、無形資産の減損損失、および、条件付対価による負債の公正価値測定の見積り変更に関連する費用または収益が含まれます。
4 調整項目に対する見積法人税の影響が含まれます。さらに2021年度通期の金額には、特定の連邦所得税問題の解決に関連した2億700万ドルの法人税額の減少が含まれます。
# # #
MSDについて
MSD(Merck & Co., Inc., Kenilworth, N.J., U.S.A.が米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、130年にわたり、人々の生命を救い、人生を健やかにするというミッションのもと、世界で最も治療が困難な病気のために、革新的な医薬品やワクチンの発見、開発、提供に挑みつづけてきました。MSDはまた、多岐にわたる政策やプログラム、パートナーシップを通じて、患者さんの医療へのアクセスを推進する活動に積極的に取り組んでいます。私たちは、今日、がん、HIVやエボラといった感染症、そして新たな動物の疾病など、人類や動物を脅かしている病気の予防や治療のために、研究開発の最前線に立ち続けています。MSDは世界最高の研究開発型バイオ医薬品企業を目指しています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)やFacebook、Twitter、YouTubeをご参照ください。