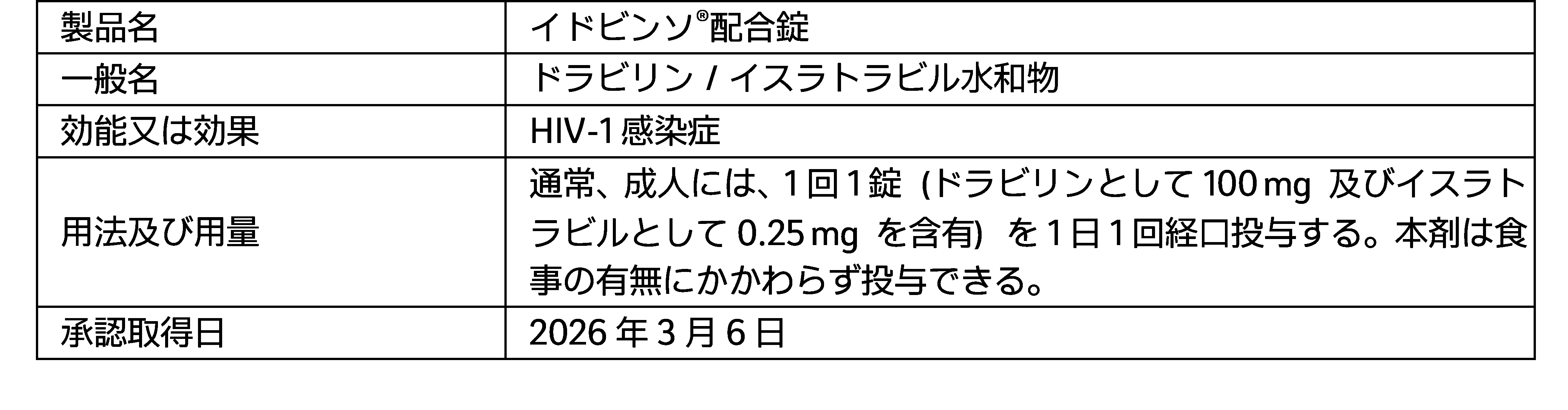1日1回1錠経口投与のHIV-1感染症治療薬「イドビンソ®配合錠」の承認を取得~新規作用機序のヌクレオシド系逆転写酵素トランスロケーション阻害剤(NRTTI)イスラトラビルと非ヌクレオシド系逆転写酵素阻害剤(NNRTI)ドラビリンの2剤配合錠~
2026/03/06 15:00 JST
報道関係各位
MSD株式会社
MSD株式会社(本社:東京都千代田区、代表取締役社長:プラシャント・ニカム、以下「MSD」)は、
本日、1日1回1錠経口投与のヒト免疫不全ウイルス1型(HIV-1)の治療薬*1として、「イドビンソ®配合錠」(一般名:ドラビリン・イスラトラビル水和物配合錠、以下「イドビンソ®」)の製造販売承認を取得しましたのでお知らせいたします。イドビンソ®は、逆転写酵素の転移阻害や、遅延型のDNA鎖伸長停止を含む複数の作用機序によってHIV-1の複製を阻害する、新規作用機序のヌクレオシド系逆転写酵素トランスロケーション阻害剤(NRTTI)であるイスラトラビルと、非ヌクレオシド系逆転写酵素阻害剤(NNRTI)であるドラビリンの2剤配合錠で、世界に先駆けて初めて日本で承認されました。
イスラトラビルは、ヤマサ醤油株式会社(本社:千葉県銚子市)とのライセンス契約に基づいて当社が開発した新規のNRTTIです。ドラビリンは、当社が開発したNNRTIで、国内では「ピフェルトロ®」として、「HIV-1感染症」の効能又は効果で承認されています。
HIV感染症は、HIVがCD4陽性リンパ球などの免疫担当細胞に感染することで、免疫系が徐々に破壊されエイズ(後天性免疫不全症候群)を発症する進行性の疾患です。日本では、HIV感染者およびエイズ患者数は毎年1,000人前後の新規報告があり、両者の合計は累計で36,381人(2024年末現在、凝固因子製剤による感染例を除く)とされています*2。HIV感染症の治療は、原則として血中のウイルス量を検出限界以下に抑え続けることを目標に行われ、適切な抗HIV薬を継続して服用することが必要となります。しかしながら、抗HIV療法によって予後が改善し、治療が長期化することに伴い、さまざまな合併症が新たな問題となってきています*3。そのため、一人ひとりの健康上のニーズに対応できる幅広い選択肢が求められています。
イドビンソ®は、HIV-1感染症患者さんのニーズの変化に対応する新たな治療選択肢となることが期待されます。また、イドビンソ®は、抗HIV療法によりウイルス学的抑制が得られている成人HIV-1感染症に対する有効性および安全性が確認され、1日1回1錠の経口投与配合剤であり食事の影響を受けずに投与可能であることから、アドヒアランスの維持が期待されます。
MSDは、HIV感染症領域において、日本では1997年にクリキシバンを発売して以来、約30年間にわたり数々の革新的な治療薬を届けてまいりました。引き続き、患者さんや医療従事者のHIV治療におけるニーズに応えてまいります。
*1 効能又は効果「HIV-1感染症」、効能又は効果に関する注意「ウイルス学的失敗の経験がなく、切り替え前3カ月間以上ウイルス学的抑制(HIV-1 RNA量が50 copies/mL未満)が得られており、ドラビリン又はイスラトラビルに対する耐性関連変異を持たず、本剤への切り替えが適切であると判断される抗HIV-1薬既治療成人患者」
*2 厚生労働省エイズ動向委員会 令和6(2024)年エイズ発生動向年報
*3 HIV感染症および血友病におけるチーム医療の構築と医療水準の向上を目指した研究班 抗HIV治療ガイドライン 2025年3月
承認の根拠となった臨床試験について
国際共同第Ⅲ相試験(051試験)
本試験は、ウイルス学的抑制(HIV-1 RNA 量50 copies/mL 未満)が3カ月間以上得られており、ウイルス学的失敗の経験がないHIV-1感染症成人患者を対象に、抗レトロウイルス療法(ART)の継続投与レジメンから「イドビンソ®」1日1回へ切り替えた際の有効性および安全性を評価する無作為化、非盲検、実薬対照試験です。治験参加者553例(日本人13例を含む)は、2:1の比で「イドビンソ®」切替え群(368例)またはベースライン ART 継続群(185例)に無作為に割り付けられました。
有効性の主要評価項目である48週時のHIV-1 RNA量が50 copies/mL以上の参加者の割合は、「イドビンソ®」切替え群5例(1.4%)、ベースラインART継続群9例(4.9%)で、「イドビンソ®」はベースラインART継続群に対する非劣性が検証されました(非劣性マージン:群間差の多重性を調整した両側95%CIの上限が4%未満)。48週時点で、「イドビンソ®」を投与した366例中44例(12.0%)に副作用が認められ、主な副作用は下痢12例(3.3%)、疲労および浮動性めまい各7例(1.9%)、腹部膨満、体重増加および頭痛各6例(1.6%)でした。
国際共同第Ⅲ相試験(052試験)
本試験は、ウイルス学的抑制(HIV-1 RNA 量50 copies/mL 未満)が3カ月間以上得られており、ウイルス学的失敗の経験がないHIV-1感染症成人患者を対象に、ビクテグラビル/エムトリシタビン/テノホビルアラフェナミド(BIC/FTC/TAF)の継続投与レジメンから「イドビンソ®」1日1回へ切り替えた際の有効性および安全性を評価する無作為化、二重盲検、実薬対照試験です。治験参加者514例(日本人17例を含む)は、2:1の比で「イドビンソ®」切替え(1日1回)群(343例)または BIC/FTC/TAF 継続群(171例)に無作為に割り付けました。
有効性の主要評価項目である48週時点のHIV-1 RNA量が50 copies/mL以上の被験者割合は、「イドビンソ®」切替え群5例(1.5%)、BIC/FTC/TAF継続群1例(0.6%)で、「イドビンソ®」はBIC/FTC/TAFに対する非劣性が検証されました(非劣性マージン:群間差の多重性を調整した両側95%CIの上限が4%未満)。48週時点で、「イドビンソ®」を投与した342例中35例(10.2%)に副作用が認められ、主な副作用は下痢5例(1.5%)、鼓腸、頭痛、そう痒症各4例(1.2%)でした。
以上
MSDについて
MSD(Merck & Co., Inc., Rahway, NJ, USAが米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、「最先端のサイエンスを駆使して、世界中の人々の生命を救い、生活を改善する」というパーパスのもとに結束し、130年以上にわたり、重要な医薬品やワクチンの開発を通して人類に希望をもたらしてきました。私たちは、世界トップクラスの研究開発型バイオ医薬品企業を目指し、人類や動物の疾患予防や治療に寄与する革新的なヘルスケア・ソリューションを提供するために、研究開発の最前線で活動しています。また、私たちは、多様かつ包括的な職場環境を醸成し、世界中の人々と地域社会に安全で持続可能かつ健康な未来をもたらすため、責任ある経営を日々行っています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)やFacebook、Instagram、YouTubeをご参照ください。
<参考資料>