Merck & Co., Inc., Rahway, NJ, USA 2025年度第3四半期決算発表
2025/11/27 11:00 JST
報道関係各位
MSD株式会社
この参考資料は、Merck & Co., Inc., Rahway, NJ, USAが2025年10月30日付(米国東部時間)に発表した2025年度第3四半期決算のプレスリリースMerck & Co., Inc., Rahway, N.J., USA Announces Third-Quarter 2025 Financial Results – Merck.comを日本語に翻訳したもので、内容および解釈については英語が優先されます。
以下の医療用医薬品は、日本国内で発売しております。カナ表記は括弧内をご参考ください。 BRIDION®(ブリディオン®)、CAPVAXIVE™(キャップバックス®)、GARDASIL®(ガーダシル®)、GARDASIL®9(シルガード®9)、JANUVIA®(ジャヌビア®)、KEYTRUDA®(キイトルーダ®)、LAGEVRIO™(ラゲブリオ®)、Lenvima®(レンビマ®)、Lynparza®(リムパーザ®)、PREVYMIS®(プレバイミス®)、VAXNEUVANCE®(バクニュバンス®)、WELIREG™(ウェリレグ®)、WINREVAIR™(エアウィン®)
参考資料
Merck & Co., Inc., Rahway, NJ, USA
2025年度第3四半期決算発表
- 2025年度第3四半期の全世界売上高は、前年同期比4%増の173億ドル(為替変動の影響を除き3%増の成長)
- KEYTRUDAの売上高は、10%の成長で81億ドル(為替の影響を除き8%増)
- WINREVAIRの売上高は、名目および為替影響を除いて141%の成長で3億6,000万ドル
- CAPVAXIVEの売上高は2億4,400万ドル
- GARDASILおよびGARDASIL 9の売上高は、24%減で17億ドル(為替の影響を除き25%減)
- アニマルヘルスの売上高は、9%の成長で16億ドル(為替の影響を除き7%増)
- 2025年度第3四半期のGAAPベースのEPSは2.32ドル、non-GAAPベースでは2.58ドル。GAAPおよびnon-GAAPベースのEPSは、MK-2010に関する技術移転に伴うLaNova社へのマイルストーン支払に関連する費用0.10ドル(一株当たり)を含む
- KEYTRUDAで承認されているすべての固形がんを適応症とするKEYTRUDA QLEX皮下注射剤がFDAの承認を取得
- 2025年ESMO年次総会において、KEYNOTE-905試験およびKEYNOTE-B96試験の良好な生存期間のデータを含む、20種類以上のがんおよび複数の治療法に関連する新規の研究成果を発表
- 成人向けの高コレステロール血症治療を目的としたEnlicitide Decanoateの3番目の第3相試験CORALreef Lipids試験のトップライン結果が良好であることを発表
- ファーストインクラスの成人向けCOPD維持療法薬 OHTUVAYREを有するVerona Pharma社の買収を10月に完了
- 2025年通期の業績見通し
- 2025年度通期の全世界売上高を645億ドル~650億ドルと予想
- 2025年度通期のnon-GAAPベースのEPSレンジを8.93ドル~8.98ドルに修正
米国ニュージャージー州ローウェイ– Merck & Co., Inc., Rahway, NJ, USA(米国とカナダ以外ではMSD)は2025年10月30日(米国東部時間)、2025年度第3四半期決算を発表しました。
会長兼最高経営責任者(CEO)のロバート・M・デイビスは、「当四半期決算では、重要なパイプラインの進捗に注力した戦略を引き続き実行し、主要な承認および新規製剤の上市の成功をもたらしました。当社の革新的な治療薬およびワクチンのポートフォリオを通して、患者さんと顧客に大きな価値を提供していきます。また、Verona Pharma社の買収完了など説得力のある戦略的な事業開発や米国の製造部門および研究開発費の拡大を通して、私たちのパイプラインに対する有力な投資を行うことで将来に確かな自信を感じています。私たちは順次、マイルストーンを達成することにより新しいステージの扉を開き、さらなる成功に導く良好なポジションを保持しているものと確信しています」と述べています。
決算サマリー

2025年第3四半期のGAAP(GAAP:一般に公正妥当と認められる会計基準)ベースの希薄化後EPSは2.32ドル、non-GAAPベースのEPSは2.58ドルでした。2025年第3四半期のGAAPおよびnon-GAAPベースの EPSには、MK-2010に関する技術移転に伴うLaNova Medicines(LaNova社、Sino Biopharmaceutical Limited によって買収)へのマイルストーン支払に関連する費用0.10ドル(一株当たり)が含まれています。2024年第3四半期のGAAPおよびnon-GAAPベースのEPSには、Eyebiotech Limited(EyeBio社)の買収および関連する開発マイルストーン、Curon Biopharmaceutical(Curon社)のMK-1045の買収に関連する合計の正味費用0.79ドル(一株当たり)、ならびにgocatamig(MK-6070)を含む既存の開発・商業化契約の拡大に関連する第一三共からの支払金を反映しています。
両期のnon-GAAPベースのEPSは、事業統合・売却関連費用、事業再構築プログラムに関連する費用、および株式の投資による収益と損失を除外しています。また2025年第3四半期のnon-GAAPベースのEPSは、監査引当金調整に関連する税費用を除外しています。
2025年度第3四半期の業績
以下の表は当社の売上高上位製品および主要な製品の売上高総額を表しています。
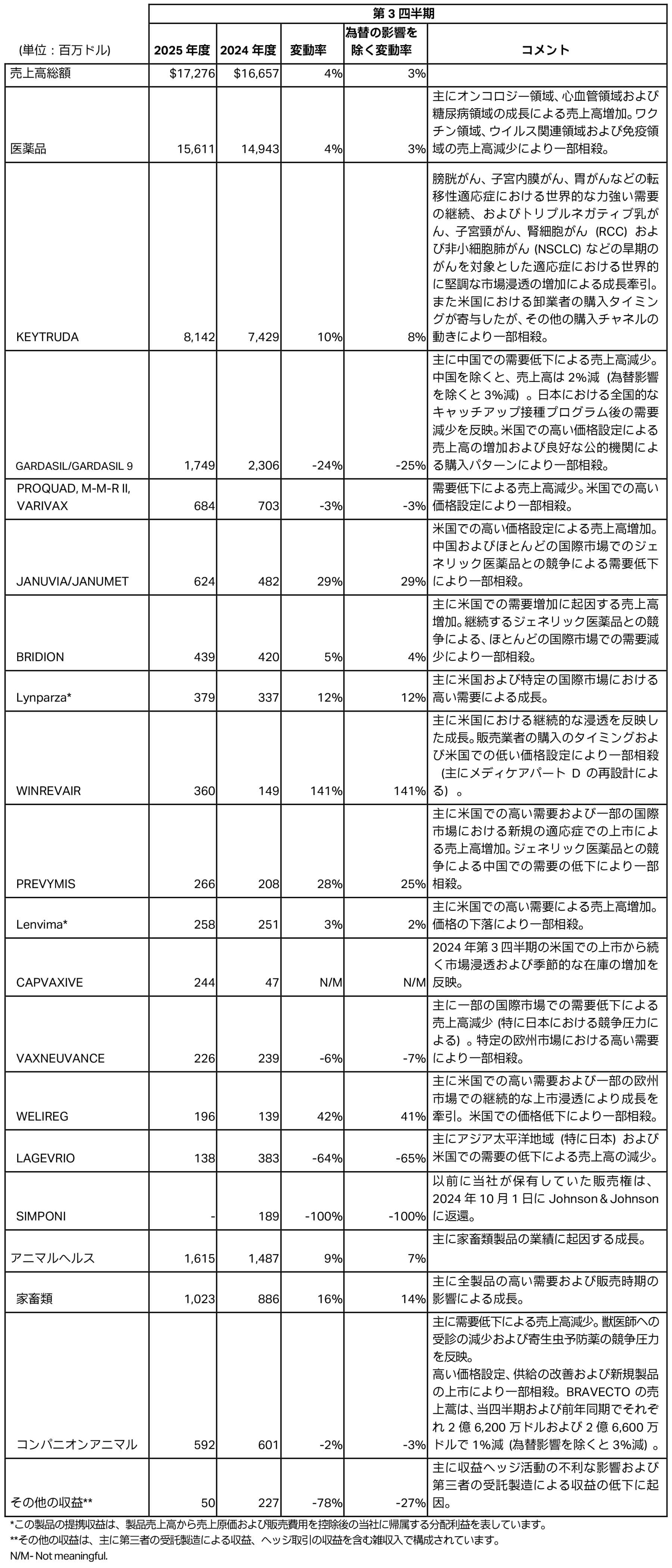
Koselugoに関する提携収益は、2024年第3四半期の3,900万ドルに対し2025年第3四半期は2億1,400万ドルでした。この増加は、AstraZenecaとの提携契約を変更したためであり(当社とAstraZenecaで収益と費用の分担する規定を廃止した)、その支払体系が変更されたことから、1億5,000万ドルの前払金および5,000万ドルの承認申請上のマイルストーンが発生しました。
2025年度第3四半期の費用、EPSおよび関連情報
以下の表は、費用に関する抜粋情報を表しています。
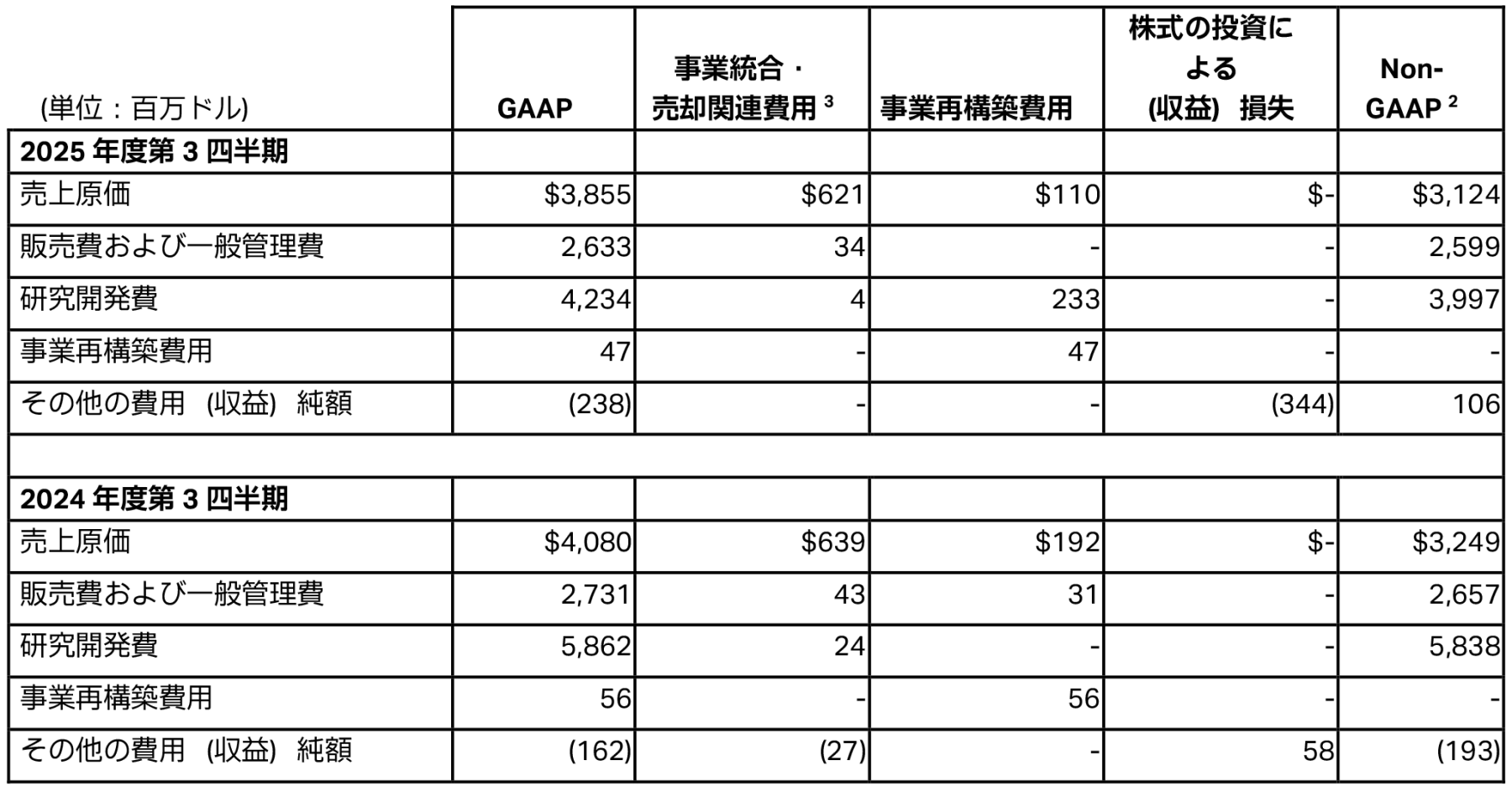
GAAPベースの費用、EPSおよび関連情報
GAAPベースの売上総利益率は、2024年第3四半期の75.5%に対し2025年第3四半期は77.7%でした。この増加は主に、プロダクト・ミックスによるプラス影響および事業再構築費用の減少を反映していますが、在庫の減損処理の増加および為替のマイナス影響により一部相殺されました。
2025年第3四半期の販売費および一般管理費(SG&A)は26億ドルで、2024年第3四半期と比べて4%減少しました。この減少は主に管理費、事業再構築費用および販売促進費の減少によるものですが、為替のマイナス影響により一部相殺されました。
2025年第3四半期の研究開発費(R&D)は42億ドルで、2024年第3四半期と比べて28%減少しました。この減少は主に、事業開発活動に関連する費用の減少を反映しています。2024年第3四半期ではEyeBio社およびMK-1045の買収に関連する合計の費用22億ドルに対して、2025年第3四半期ではMK-2010に関する技術移転の完了に伴うLaNova社へのマイルストーン支払に関連する費用3億ドルが含まれています。これらの費用を除くと、研究開発費は主に、事業再構築費用および臨床開発費の増加により増加しています。
2025年第3四半期のその他の費用(収益)純額は2億3,800万ドルの収益、2024年第3四半期は1億6,200万ドルの収益でした。このプラス影響は主に、2024年における株式の投資による損失に対して、2025年は株式の投資による利益が計上されたことを反映していますが、gocatamig(MK-6070)を含む既存の開発・商業化契約の拡大に関連する第一三共からの支払金として2024年に認識された1億7,000万ドルの収益により一部相殺されました。
2025年度第3四半期の実効税率は14.2%でした。
2025年第3四半期のGAAPベースのEPSは2.32ドル、2024年第3四半期は1.24ドルでした。この増加は主に、EyeBio社、Curon社および第一三共との事業活動に関連する合計の正味費用0.79ドル(一株当たり)によるものですが、2025年における技術移転の完了に伴うLaNova社へのマイルストーン支払に関連する費用0.10ドル(一株当たり)により一部相殺されました。
non-GAAPベースの費用、EPSおよび関連情報
2025年第3四半期のnon-GAAPベースの売上総利益率は81.9%、2024年第3四半期は80.5%でした。この増加は主に、プロダクト・ミックスによるプラス影響を反映していますが、在庫の減損処理の増加および為替のマイナス影響により一部相殺されました。
2025年第3四半期のnon-GAAPベースの販売費および一般管理費(SG&A)は26億ドルで、2024年第3四半期と比べて2%減少しました。この減少は主に管理費および販売促進費の減少によるものですが、為替のマイナス影響により一部相殺されました。
2025年第3四半期のnon-GAAPベースの研究開発費(R&D)は40億ドルで、2024年第3四半期と比べて32%減少しました。この減少は主に、事業開発活動に関連する費用の減少を反映しています。2024年第3四半期ではEyeBio社およびMK-1045の買収に関連する合計の費用22億ドルに対して、2025年第3四半期ではMK-2010に関する技術移転の完了に伴うLaNova社へのマイルストーン支払に関連する費用3億ドルが含まれています。これらの費用を除くと、研究開発費は主に、臨床開発費の増加により増加しています。
2025年第3四半期のnon-GAAPベースのその他の費用(収益)純額は1億600万ドルの費用、2024年第3四半期は1億9,300万ドルの収益でした。このマイナス影響は主に、gocatamig(MK-6070)を含む既存の開発・商業化契約の拡大に関連する第一三共からの支払金として2024年に認識された1億7,000万ドルの収益を反映しています。
2025年第3四半期のnon-GAAPベースの実効税率は13.4%でした。
2025年第3四半期のnon-GAAPベースのEPSは2.58ドル、2024年第3四半期は1.57ドルでした。この増加は主に、EyeBio社、Curon社および第一三共との事業活動に関連する合計の正味費用0.79ドル(一株当たり)によるものですが、2025年における技術移転の完了に伴うLaNova社へのマイルストーン支払に関連する費用0.10ドル(一株当たり)により一部相殺されました。
当期純利益およびEPSのGAAPベースからnon-GAAPベースへの調整は、以下の表のとおりです。
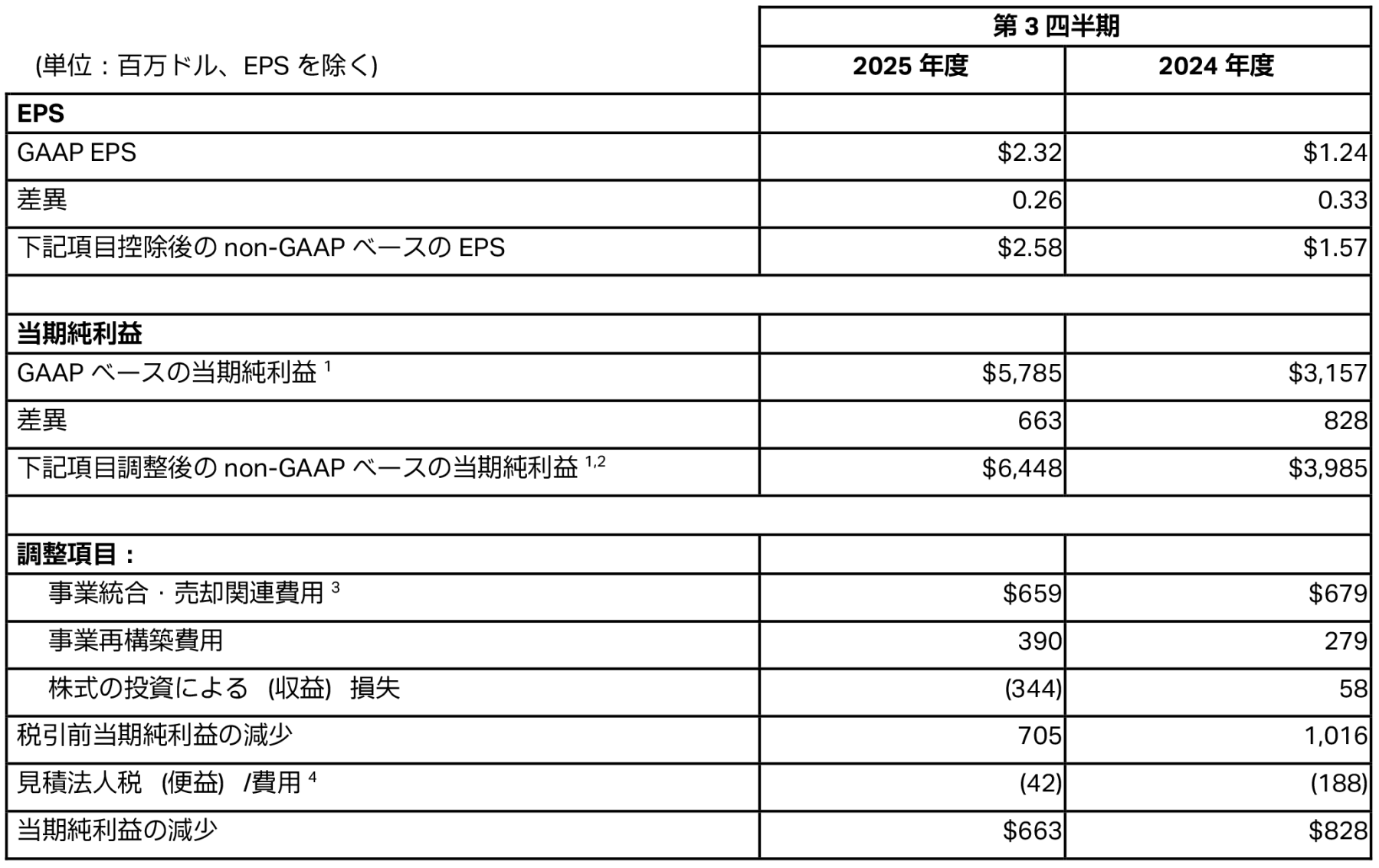
パイプラインおよびポートフォリオハイライト
2025年第3四半期において、当社は主要な規制および臨床のマイルストーンを達成し、パイプラインの前進を継続しました。
オンコロジー領域では、2025年9月に米国食品医薬品局(FDA)は、第3相MK-3475A-D77試験の結果に基づき、成人患者を対象にKEYTRUDAで承認されている大部分の固形がんを適応症とするKEYTRUDA QLEX皮下(SC)注射剤を承認しました。その後、2025年10月、第3相KEYNOTE-689試験の結果に基づき、切除可能な局所進行頭頸部扁平上皮がん(LA-HNSCC)の特定の成人患者の治療においてもKEYTRUDA QLEX注射剤を承認しました。現在、KEYTRUDA QLEX注射剤は、成人患者を対象にKEYTRUDAで承認されているすべての固形がんを適応症に承認されています。これは、初めてかつ唯一の、医療従事者によってわずか1分で投与することが可能な免疫チェックポイント阻害薬の皮下注射剤です。
さらに欧州医薬品庁(EMA)の欧州医薬品委員会(CHMP)は、すべての成人患者に対する適応としてKEYTRUDAの皮下注射の承認を推奨する肯定的な見解を採択しました(2025年第4四半期に最終決定を予定)。また欧州委員会(EC)は、PD-L1陽性の切除可能なLA-HNSCC治療の周術期レジメンの一部としてKEYTRUDAを承認しました。
2025年欧州臨床腫瘍学会(ESMO)年次総会では、新規の腫瘍タイプおよび早期ステージの疾患における進展に注力し、差別化された幅広いポートフォリオとパイプラインに基づく新たな研究成果を発表しました。これには、シスプラチン不適格の筋層浸潤性膀胱がん(MIBC)患者を対象とした第3相KEYNOTE-905試験(EV-303とも呼ばれる)、プラチナ抵抗性再発卵巣がん患者を対象とした第3相KEYNOTE-B96試験および特定のプラチナ抵抗性卵巣がん患者を対象とした第2/3相REJOICE-Ovarian01試験(第一三共株式会社との提携)の良好な結果、進行子宮体がん患者を対象とした第3相KEYNOTE-775試験の長期フォローアップデータ、ならびに早期および転移性のNSCLC患者を対象としたKEYTRUDAの長期データが含まれました。
ワクチンおよび感染症領域では、2025年8月に日本で2剤の承認を取得しました:SILGARD 9の商標の下で販売されている9価HPVワクチンの9歳以上の男性への対象拡大と、高齢者または肺炎球菌感染症の罹患リスクが高い成人を対象としたCAPVAXIVEです。
欧州エイズ臨床学会2025年カンファレンスでは、ウイルス学的抑制が得られているHIV-1感染症成人患者を対象に開発中の1日1回経口投与のドラビリン/イスラトラビル2剤配合錠を評価した第3相試験2試験による新規のデータを発表しました。いずれの臨床試験においても、体重および体組成は最小限の変動であり、空腹時脂質およびインスリン抵抗性の恒常性モデル評価では臨床的に意義のある影響は認められませんでした。
循環器領域では、当社は第3相CORALreef Lipids試験のポジティブなトップライン結果を発表しました。これは、高コレステロール血症の成人患者を対象に、開発中の1日1回経口投与のプロ蛋白転換酵素サブチリシン/ケキシン9型(PCSK9)阻害剤 enlicitide decanoate の安全性と有効性を評価する試験です。この試験では、すべての主要評価項目と主要な副次評価項目が達成されました。Enlicitideは、初めての経口PCSK9阻害剤となることが期待されています。
さらに、FDAは第3相ZENITH試験の結果に基づき、WINREVAIRの米国製品ラベル更新を承認しました。これにより、肺動脈性肺高血圧症(PAH)による入院、肺移植および死亡などの臨床的増悪イベントを含む適応に拡大されました。また2025年欧州呼吸器学会年次総会では、新たにPAH(WHO Group 1)と診断された、WHO機能分類(FC)II度またはIII度で、疾患進行のリスクが中から高の成人患者(18歳以上)を対象として、WINREVAIRをプラセボと比較評価する(いずれもバックグラウンド治療と併用)第3相HYPERION試験の良好な結果を発表しました。これによりPAHの診断から1年以内のWINREVAIR投与は、プラセボと比較して臨床的悪化イベントのリスクを有意に軽減することが示されました。
当社は、2025年10月にVerona Pharma plc(Verona Pharma社)の買収を完了しました。これにより、Ohtuvayreが加わることで心肺系のポートフォリオが強化されます。FDAは、成人の慢性閉塞性肺疾患(COPD)のファーストインクラスの維持療法薬としてOhtuvayreを承認しました。
以下の表は、当社のパイプラインおよびポートフォリオに関する重要な最新ニュースリリースを表しています。詳細は当社ウェブサイトのニュースリリースセクション*をご覧ください。
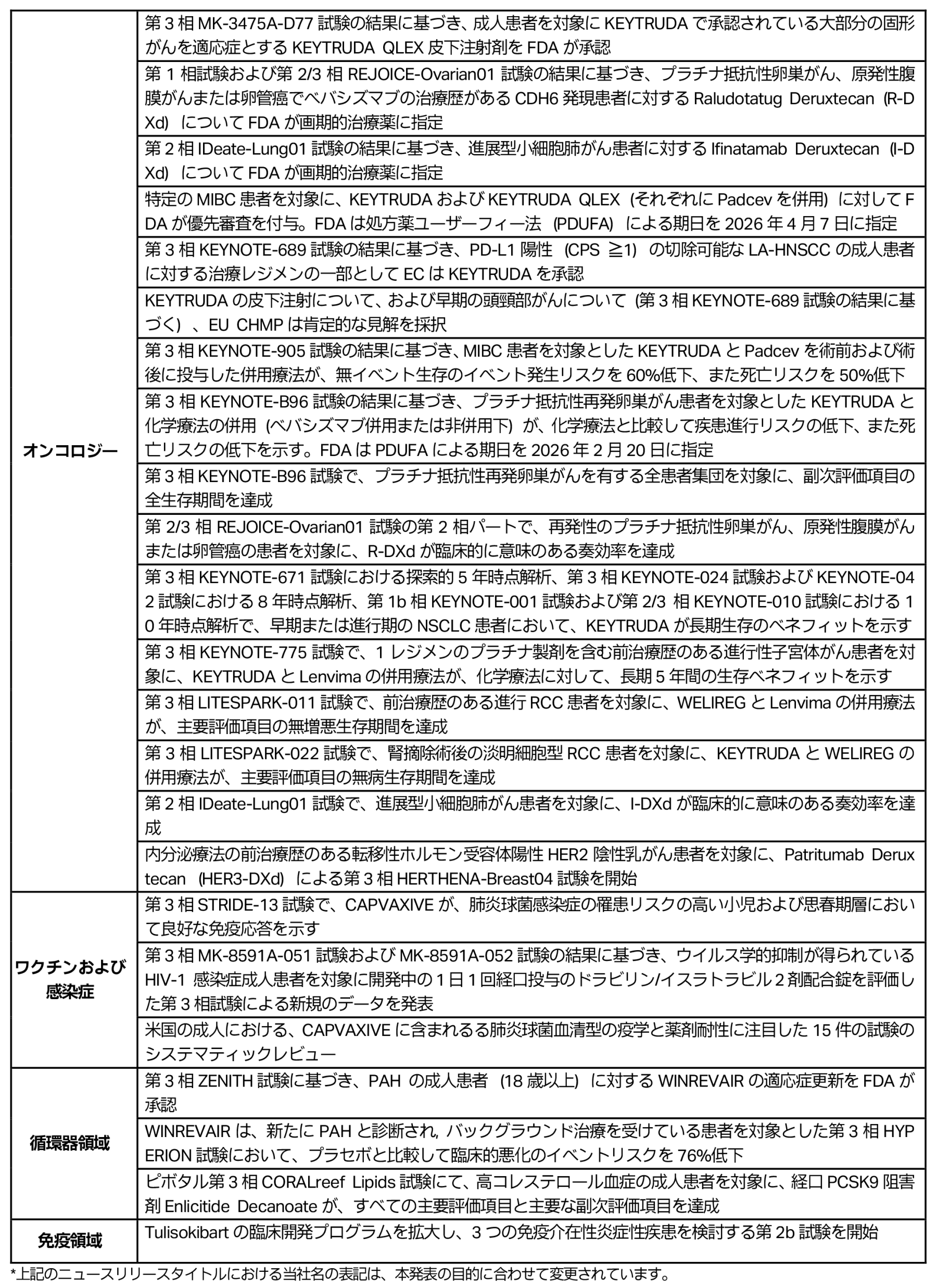
製造および研究開発投資
当社は、米国における製造および研究開発能力への長期投資を続けています。バージニア州エルクトンに30億ドル規模の医薬品製造拠点(センター・オブ・エクセレンス)の建設を開始しました。これは40万平方フィートの施設であり、医薬品の有効成分および製剤を製造するほか、低分子医薬品の製造支援や試験設備への投資、500人を超えるフルタイム雇用を創出する予定です。この投資は、2025年から国内の製造および研究開発を拡大させることを目的に700億ドル超を拠出するコミットメントの一環です(研究開発における将来の事業開発を含めず)。バイオ医薬品イノベーション分野におけるグローバルリーダーとして米国の長期の成長と強化をもたらします。
投資家向けイベントに関する最新情報
2025年11月7日から10日に開催される、アメリカ心臓協会(AHA)の科学セッション2025にて、当社は、革新的な心血管系パイプラインおよびポートフォリオに関する新規データを発表します。当社は、AHAの科学セッション2025に関する投資家向けイベントを11月9日午後6時(日曜)に主催する予定です。同イベントは、米国ニューオーリンズで開催され、ライブオーディオウェブキャストでアクセス可能です。
サステナビリティハイライト
私たちは「2024/2025 Purpose for Progress Impact Report」を発行しました。これは、人々の健康とアニマルへルスのために革新的なサイエンスを追求する取り組み、そして、その取り組みが重要かつ持続可能な価値を生み出すことを包括的に示すものです。また、このレポートでは、2024年に世界の4億5,000万人以上の人々に、当社の治療薬およびワクチンが届けられたことも報告しています。
2025年通期の業績見通し
以下の表は、当社の2025年通期の業績見通しの要約を表しています。
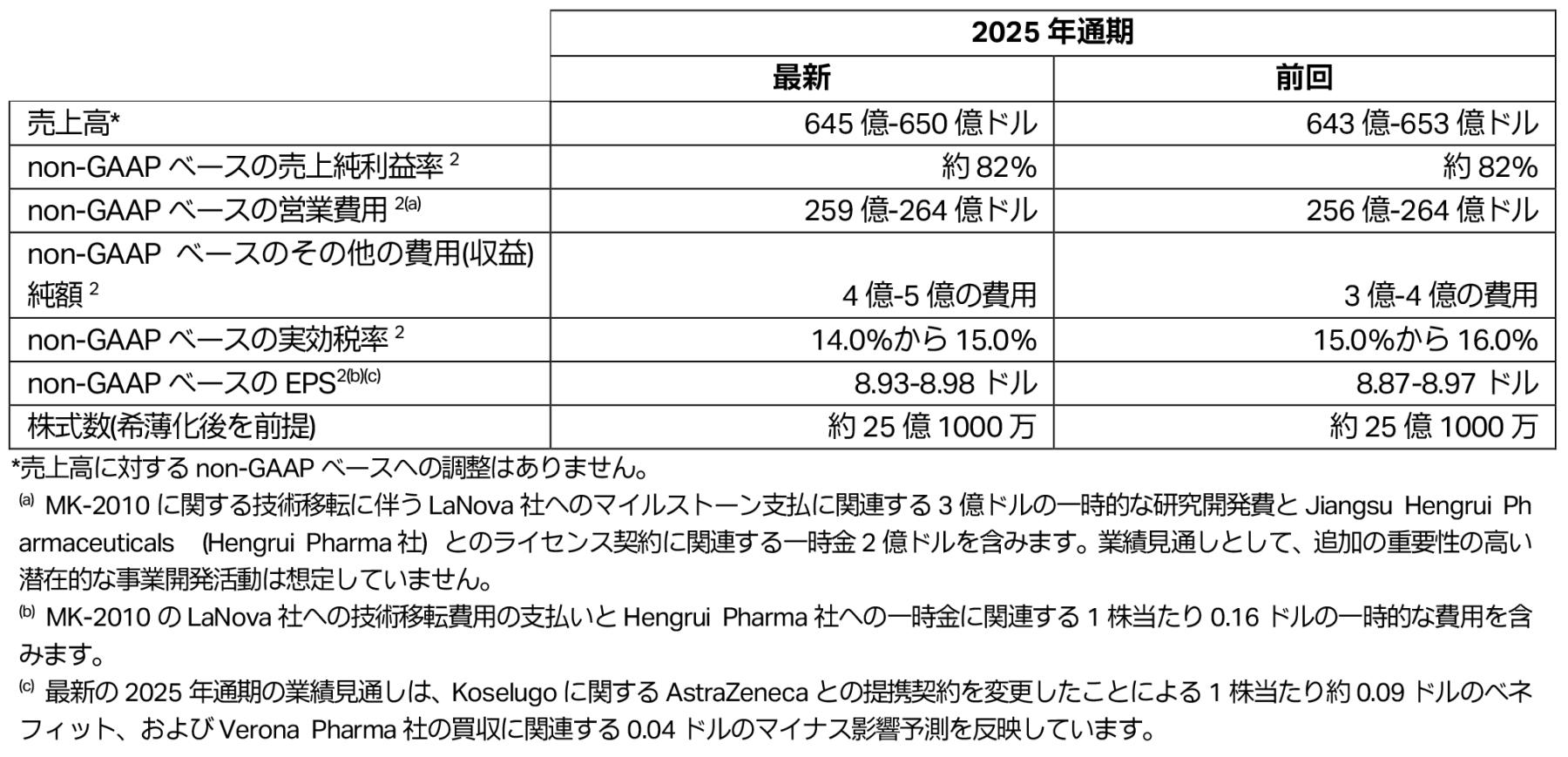
将来の見通しとしてのnon-GAAPベースの売上総利益率、non-GAAPベースの営業費用、non-GAAPベースのその他の費用(収益)純額、non-GAAPベースの実効税率、およびnon-GAAPベースのEPSに関して、最も直接的に比較を可能とするGAAPベースの指標への調整は提示していません。このような調整には、無形資産の減損損失、法的な和解、ならびに株式の投資による利益/損失(直接所有または投資ファンドによる所有権)などを含みますが、合理的な確実性をもとに調整金額を予測することができないからです。これらの項目は、本質的に予測が困難であり、当社における将来のGAAPベースの業績に重大な影響を及ぼす可能性があります。
2025年通期の売上高については、2025年10月中旬の為替レートによる約0.5%の為替のマイナス影響を含み、645億ドル~650億ドルになると予想しています。
当社は、2025年度通期のnon-GAAPベースの実効税率は、14.0%から15.0%になると予想しています。
当社は、2025年通期のnon-GAAPベースの EPSレンジを8.93ドル~8.98ドルになると予想しています。これには、1株当たり約0.15ドルの為替のマイナス影響が含まれています。この修正後のGAAPベースのEPSの業績見通しは、Koselugoに関するAstraZenecaとの提携契約を変更したこと、有利な税率予測や関税の影響に関連してコスト予測の低下を含む事業改善などによるベネフィットを反映していますが(過去の業績見通しには反映していません)、Verona Pharma社の買収に関連するマイナス影響予測および為替のマイナス影響の増大により一部相殺されました。この修正後のnon-GAAPベースのEPSレンジの中心値は、前回の業績見通しの中心値と比較して1株当たり0.04ドルの純増を反映しています。
すでに公表されているように、修正後の2025年通期のnon-GAAPベースの EPSレンジは、Hengrui Pharma社とのライセンス契約に関連する一時的な費用と、MK-2010に関するLaNova社との技術移転の完了による影響を反映しています(合計約0.16ドルのEPSへの影響)。2024年には、特定の資産買収、ライセンス契約および提携に関連する1株当たり1.28ドルの純費用により、7.65ドルのnon-GAAPベースのEPSがマイナスの影響を受けました。
過去の慣行と一貫性を保つため、財務見通しとして、追加の重要性の高い未確定の事業開発活動は想定していません。
コンファレンス・コール
Merck & Co., Inc., Rahway, NJ, USAの投資家、メディア関係者および一般の方々へのコンファレンス・コールのライブ・ウェブキャストが米国東部時間の2025年10月30日木曜日の午前9時に行われました。売上高と利益のニュースリリース、財務状況の開示追補、決算ハイライトスライドを含むウェブキャストは、www.merck.comにてご覧いただくことができます。
すべての参加者は、(800) 369-3351(フリーダイヤル、米国およびカナダ)または(517) 308-9448からアクセスコード番号9818590にてご参加いただけます。
Merck & Co., Inc., Rahway, NJ, USAについて
Merck & Co., Inc., Rahway, NJ, USA(米国とカナダ以外ではMSD)は、最先端のサイエンスを駆使して、世界中の人々の生命を救い、生活を改善するというパーパスのもとに結束しています。130年以上にわたり、重要な医薬品やワクチンの発見を通して人類に希望をもたらしてきました。私たちは、世界トップクラスの研究開発型バイオ医薬品企業を目指し、人類や動物の疾患予防や治療に寄与する革新的なヘルスケア・ソリューションを提供するために、研究開発の最前線で活動しています。私たちは、多様かつ包括的な職場環境を醸成し、世界中の人々と地域社会に、安全で持続可能かつ健康な未来をもたらすため、責任ある経営を日々続けています。
Merck & Co., Inc., Rahway, NJ, USAの将来に関する記述
このニュースリリースには、米国の1995年私的証券訴訟改革法(the Private Securities Litigation Reform Act of 1995)の免責条項で定義された「将来に関する記述」が含まれています。これらの記述は、Merck & Co., Inc., Rahway, NJ, USAの経営陣の現時点での信条と期待に基づくもので、相当のリスクと不確実性が含まれています。新薬パイプラインに対する承認取得またはその製品化による収益を保証するものではありません。予測が正確性に欠けていた場合またはリスクもしくは不確実性が現実化した場合、実際の成果が、将来に関する記述で述べたものと異なる場合も生じます。
リスクと不確実性には、業界の一般的な状況および競争環境、金利および為替レートの変動などの一般的な経済要因、米国および世界における医薬品業界の規制やヘルスケア関連の法制度が及ぼす影響、ヘルスケア費用抑制の世界的な傾向、競合他社による技術的進歩や新製品開発および特許取得、承認申請などの新薬開発特有の問題、Merck & Co., Inc., Rahway, NJ, USAによる将来の市況予測の正確性、製造上の問題または遅延、国際経済および政府の信用リスクなどの金融不安、革新的製品に対するMerck & Co., Inc., Rahway, NJ, USAの特許権やその他の保護の有効性への依存、特許訴訟や規制措置の対象となる可能性等がありますが、これらに限定されるものではありません。
Merck & Co., Inc., Rahway, NJ, USAは、新たな情報、新たな出来事、その他いかなる状況が加わった場合でも、将来に関する記述の更新を行う義務は負いません。将来に関する記述の記載と大きく異なる成果を招くおそれがあるこの他の要因については、Merck & Co., Inc., Rahway, NJ, USAに関するForm 10-Kの2024年度年次報告書および米国証券取引委員会(SEC)のインターネットサイト(www.sec.gov)で入手できるSECに対するその他の書類で確認できます。
補足資料
製品名と有効成分を以下に提示します。
医薬品
BRIDION (スガマデクス)
CAPVAXIVE (21価肺炎球菌結合型ワクチン)
GARDASIL (組換え沈降4価[6,11,16,18型]ヒトパピローマウイルス様粒子ワクチン)
GARDASIL 9 (組換え沈降9価ヒトパピローマウイルス様粒子ワクチン)
JANUMET(シタグリプチン/メトホルミン)
JANUVIA (シタグリプチン)
KEYTRUDA(ペムブロリズマブ)
KEYTRUDA QLEX (ペムブロリズマブおよびベラヒアルロニダーゼアルファ-pmph)
Koselugo (セルメチニブ)
LAGEVRIO (モルヌピラビル)
Lenvima (レンバチニブ)
Lynparza (オラパリブ)
M-M-R II (麻しん-おたふくかぜー風しん混合ワクチン)
OHTUVAYRE (エンシフェントリン)
PREVYMIS (レテルモビル)
PROCQUAD(麻しんーおたふくかぜー風しんー水痘混合ワクチン)
SIMPONI (ゴリムマブ)
VARIVAX (水痘ワクチン)
VAXNEUVANCE (沈降15価肺炎球菌結合型ワクチン)
WELIREG (ベルズチファン)
WINREVAIR (ソタテルセプト)
アニマルヘルス
BRAVECTO (フルララネル)
1 Merck & Co., Inc., Rahway, N.J., USAに帰属する当期純利益。
2 Merck & Co., Inc., Rahway, NJ, USAは、特定項目の性質およびそれらが事業業績や傾向に関する分析に与える影響を考慮し、2024年度および2023年度の特定の項目の影響を除いたnon-GAAPベースの情報を提供しています。経営陣は、non-GAAPベースの決算報告を用いて業績を評価しているため、この情報が会社の業績に対する投資家の理解を深めるものと考えています。経営陣は、non-GAAPベースの指標を目標の設定や達成予測のため、またその他の基準も併用しながら当社の業績を評価するために社内的に活用します。加えて、上級管理職の報酬を含む従業員の年間報酬は、部分的にnon-GAAPベースの税引前利益をベースとして支払われています。これはGAAPに基づき算出された情報に関する追加情報であって、その代わりとなるものではなく、また優先されるものでもありません。non-GAAPベースの調整についての詳細は、本リリースに添付された表2a(脚注を含む)を参照してください。
3 事業統合・売却に関する統合費用、取引費用およびその他の費用、ならびに提携やライセンス契約に関連する無形資産の償却費と共に、事業の統合に関連する費用を反映し、無形資産の償却費、無形資産の減損損失、および、条件付対価による負債の公正価値測定の見積り変更に関連する費用または収益が含まれます。
4 non-GAAP調整の現地の法定税率を適用した、調整項目への推定税影響額が含まれています。また2025年第3四半期の金額には、監査引当金調整に関連する税費用8,600万ドルも含まれます。
MSDについて
MSD(Merck & Co., Inc., Rahway, NJ, USA.が米国とカナダ以外の国と地域で事業を行う際に使用している名称)は、「最先端のサイエンスを駆使して、世界中の人々の生命を救い、生活を改善する」というパーパスのもとに結束し、130年以上にわたり、重要な医薬品やワクチンの開発を通して人類に希望をもたらしてきました。私たちは、世界トップクラスの研究開発型バイオ医薬品企業を目指し、人類や動物の疾患予防や治療に寄与する革新的なヘルスケア・ソリューションを提供するために、研究開発の最前線で活動しています。また、私たちは、多様かつ包括的な職場環境を醸成し、世界中の人々と地域社会に安全で持続可能かつ健康な未来をもたらすため、責任ある経営を日々行っています。MSDの詳細については、弊社ウェブサイト(www.msd.co.jp)やFacebook、Instagram、YouTubeをご参照ください。

